
| A. | Hg(l)+H2SO4(aq)=HgSO4(aq)+H2(g)常温下不能自发进行,说明△H<0 | |
| B. | 在一密闭容器中发生2SO2(g)+O2(g)?2SO3(g)反应,平衡后增大压强,平衡会正向移动,$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})•c({O}_{2})}$值增大 | |
| C. | 已知25℃时,Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=2.0×10-12,所以AgCl的溶解度大于Ag2CrO4的溶解度 | |
| D. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解 |
分析 A、反应不能自发,应满足△G=△H-T•△S>0,结合反应的△H和△S进行判断;
B、平衡常数是温度的函数;
C、设AgCl溶解的浓度为xmol/L,则溶液中的银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为1.8×10-10=x×x,解得x=1.35×10-5mol/L
同理设Ag2CrO4溶解的浓度为ymol/L,则溶液中的银离子浓度为2ymol/L,氯离子也为ymol/L,再根据溶度积为2.0×10-12=(2y)2×y,解得y=0.8×10-4mol/L,故溶度积小的溶解度反而大,所以Ksp的大小与溶解能力没有一定的关系;
D、水解的过程是吸热反应.
解答 解:A、反应不能自发,应满足△G=△H-T•△S>0,即△H>T•△S,而反应的△S>0,故△H>0,故A错误;
B、平衡常数是温度的函数,所以增大压强,平衡常数不变,故B错误;
C、设AgCl溶解的浓度为xmol/L,则溶液中的银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为1.8×10-10=x×x,解得x=1.35×10-5mol/L
同理设Ag2CrO4溶解的浓度为ymol/L,则溶液中的银离子浓度为2ymol/L,氯离子也为ymol/L,再根据溶度积为2.0×10-12=(2y)2×y,解得y=0.8×10-4mol/L,故溶度积小的溶解度反而大,所以Ksp的大小与溶解能力没有一定的关系,故C错误;
D、水解的过程是吸热反应,所以沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解,故D正确;
故选D.
点评 本题考查难溶电解质的溶解平衡,本题难度中等,比较溶解度大小,若用溶度积必须是同类型,否则不能比较.


科目:高中化学 来源: 题型:选择题
| A. | 1L水中溶解5.85gNaCl所形成溶液物质的量浓度是0.1mol•L-1 | |
| B. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| C. | 标准状况下,22.4L单质溴所含有的原子数目为2NA | |
| D. | 3.4gNH3中含N-H键数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
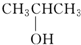 ⑨${\;}_{6}^{13}$C (填序号)
⑨${\;}_{6}^{13}$C (填序号)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
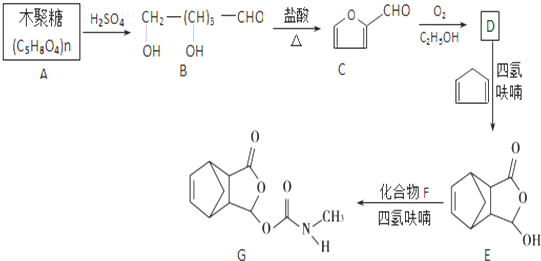
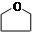 ,在流程中作反应的催化剂;
,在流程中作反应的催化剂; ;
; .
. .
. 、CH3NHCOOH或CH3N=C=O.
、CH3NHCOOH或CH3N=C=O. .
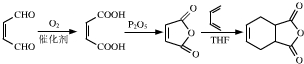
. )是合成抗病毒药物阿昔洛韦的中间体.参照上述合成路线,写出以1,3-丁二烯为原料制备H的合成路线流程图(无机试剂任用):
)是合成抗病毒药物阿昔洛韦的中间体.参照上述合成路线,写出以1,3-丁二烯为原料制备H的合成路线流程图(无机试剂任用):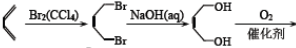
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向HA溶液中逐滴加入少量NH3•H2O,$\frac{c({H}^{+})}{c({A}^{-})}$逐渐增大 | |
| B. | 常温下,0.1mol•L-1 HA溶液中水电离的c(H+)为10-13mol•L-1 | |
| C. | NaA溶液中加入HCl溶液至恰好完全反应,存在关系:2c(Na+)=c(A-)+c(Cl-) | |
| D. | 常温下,0.1mol•L-1 NaA溶液水解常数为10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B2)=0.9mol/(L•s) | B. | v(A2)=0.5mol/(L•s) | ||
| C. | v(C)=0.62mol/(L•s) | D. | v(B2)=4.2mol/(L•min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com