
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:

相对分子质量 | 密度/(gcm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |

实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是:__________________。
(2)在洗涤操作中,第一次水洗的主要目的是:________________;第二次水洗的主要目的是:________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a. 直接将乙酸异戊酯从分液漏斗上口倒出
b. 直接将乙酸异戊酯从分液漏斗下口放出
c. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:________________________________。
(5)实验中加入少量无水MgSO4的目的是:________________________________。
(6)本实验的产率是:________________(填标号)。
a. 30% b. 40% c. 50% d. 60%
(7)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏______(填“高”或“低”),其原因是________________________________。
【答案】球形冷凝管 洗掉大部分硫酸和醋酸 洗掉碳酸氢钠 d 提高醇的转化率 干燥 d 高 会收集少量未反应的异丙醇
【解析】
根据实验步骤:A中异戊醇、乙酸在浓硫酸的催化作用下,反应生成乙酸异戊酯,由于反应是可逆反应,反应混合液是乙酸异戊酯、未反应的乙酸、未反应的异戊醇、催化剂硫酸,分别用少量水洗涤,除去乙酸和硫酸,再用饱和碳酸氢钠溶液除去未洗净的醋酸,同时降低酯的溶解度,分液,除去残留的碳酸氢钠,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,得到乙酸异戊酯粗产品,进行蒸馏纯化,得乙酸异戊酯。
(1)根据仪器构造解答;
(2)产品中混有硫酸和醋酸,可用水洗去,再加入碳酸氢钠溶液除去未洗净的醋酸,同时降低酯的溶解度,第二次水洗,主要目的是除去产品中残留的碳酸氢钠;
(3)酯与水不互溶且密度比水大,用分液操作分离;
(4)制备反应为可逆反应,根据浓度对平衡的影响分析;
(5)无水MgSO4有吸水性,作干燥剂;
(6)乙酸的物质的量为:n=6.0g÷60g·mol-1=0.1mol,异戊醇的物质的量为:n=4.4g÷88g·mol-1=0.05mol,乙酸和异戊醇是按照1:1进行反应,乙酸过量,生成乙酸异戊酯的量要按照异戊醇的物质的量计算,即理论上生成0.05mol乙酸异戊酯,再计算产率。
(7)异戊醇沸点为131℃,在进行蒸馏操作时,若从130℃便开始收集馏分,会收集少量未反应的异丙醇。
(1)仪器B为球形冷凝管;
(2)产品中混有硫酸和醋酸,可用水洗去,再加入碳酸氢钠溶液除去未洗净的醋酸,同时降低酯的溶解度,第二次水洗,主要目的是除去产品中残留的碳酸氢钠;
(3)由于酯和水二者互不相溶,水在下层,酯在上层;分液时,要先将水层从分液漏斗的下口放出,待到两层液体界面时关闭分液漏斗的活塞,再将乙酸异戊酯从上口放出,故选d;
(4)酯化反应是可逆反应,增大反应物的浓度可以使平衡正向移动;同时增加一种反应物的浓度,可以使另一种反应物的转化率提高,加入过量乙酸的目的是提高转化率;
(5)实验中加入少量无水硫酸镁吸收酯中少量的水分,对其进行干燥;
(6)乙酸的物质的量为:n=6.0g÷60g·mol-1=0.1mol,异戊醇的物质的量为:n=4.4g÷88g·mol-1=0.05mol,乙酸和异戊醇是按照1:1进行反应,乙酸过量,生成乙酸异戊酯的量要按照异戊醇的物质的量计算,即理论上生成0.05mol乙酸异戊酯,实际上生成的乙酸异戊酯的物质的量为:3.9g÷130g·mol-1=0.03mol,实验中乙酸异戊酯的产率为:0.03mol/0.05mol×100%=60%;
故选c。
(7)异戊醇沸点为131℃,在进行蒸馏操作时,若从130℃便开始收集馏分,会收集少量未反应的异丙醇,被当成产物,会使实验的产率偏高。


科目:高中化学 来源: 题型:
【题目】中国学者在水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
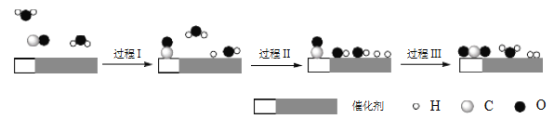
下列说法正确的是
A. 过程Ⅰ、过程Ⅲ均为放热过程
B. 过程Ⅲ生成了具有极性共价键的H2、CO2
C. 使用催化剂降低了水煤气变换反应的ΔH
D. 图示过程中的H2O均参与了反应过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏丹红一号(sudan Ⅰ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料制备的,它们的结构简式如下所示:

![]()
![]()
(苏丹红一号) (苯胺) (2—萘酚)
(提示: 可表示为
可表示为![]() )
)




(A) (B) (C) (D)
(1)苏丹红一号的化学式(分子式)为_______________________________
(2)在下面化合物(A)~(D)中,与2-萘酚互为同分异构体的有(填字母代号)_____。
(3)上述化合物(C)含有的官能团是_____________________________
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1molE与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴代物,两种一溴代物的结构简式分别是_________________________________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、P、Q为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法正确的是

A. Q的氧化物一定含有离子键和共价键 B. 最高价含氧酸的酸性:Z<Y
C. P的最低价氢化物常温常压下为液体 D. Y形成的化合物种类最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是

A. 该装置将化学能转化为电能
B. 催化剂b表面O2发生还原反应,其附近酸性增强
C. 催化剂a表面的反应是:SO2+2H2O-2e-===SO42-+4H+
D. 若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO34NO2↑+O2↑+2H2O)。

请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入三口烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三口烧瓶中气体的颜色为________,产生该气体的化学方程式是____________。
(2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为____________(填化学式)。
(3)装置B的作用是__________________________。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。
①下列对该气体的检验方法合适的是________。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶中收集的无色气体是氧气,则氧气的来源是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4溶液中含有少量Fe3+,可通过调节pH值来将Fe3+除去,下列试剂中用来调pH值最佳的是( )
A.NaOH溶液B.浓氨水C.CuO固体D.H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-。下列说法不正确的是
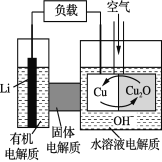
A. 放电时,Li+透过固体电解质向Cu极移动
B. 通空气时,铜被腐蚀,产生Cu2O
C. 放电时,正极的电极反应式为:Cu2O+2H+ +2 e- ===2Cu+H2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com