
反应N2(g) +3H2(g)=2NH3(g),起始时,N2的浓度为3mol·L-1,H2的浓度为5mol·L-1,3min后测得NH3浓度为0.6mol·L-1,则此时间段内,下列反应速率表示正确的是:
A.v(NH3)= 0.2mol·L-1·S-1 B. v(N2)= 1.0mol·L-1·min-1
C. v(H2)= 1.67mol·L-1·min-1 D. v(H2)= 0.3mol·L-1·min-1
科目:高中化学 来源: 题型:
下图表示298K时N2与H2反应过程中的能量变化。根据下图叙述正确的是( )
A.该反应的热化学方程式为:1/2 N2(g)+3/2 H2(g) ![]() NH3(g) △H= -92kJ·mol-1
NH3(g) △H= -92kJ·mol-1
B.不用催化剂,生成 1molNH3放出的热量为46KJ
C.加入催化剂,生成 1molNH3的反应热减小50KJ·mol-1
D.曲线b表明加入催化剂降低了反应热,加快了反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应反应N2(g)+3H2(g)2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”),在其它条件不变的情况下降低温度,逆反应速率将 (填“增大”、“减小”或“不变”) 。
(2) O2 (g)= O+2(g)+e- ![]() H1=1175.7 kJ·mol-1
H1=1175.7 kJ·mol-1
PtF6(g)+ e-1 PtF6-(g)
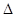 H2=- 771.1 kJ·mol-1
H2=- 771.1 kJ·mol-1
O2+PtF6-(s)=O2+(g)+PtF6- 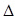 H3=482.2kJ·mol-1
H3=482.2kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6-(s)的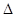 H=_____________kJ·mol-1。
H=_____________kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
查看答案和解析>>
科目:高中化学 来源:2011-2012年安徽红星中安工大附中高二下学期期中联考理科化学试卷(带解析) 题型:填空题
(6分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)在不同温度下,反应N2(g)+O2(g) 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
 2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)查看答案和解析>>
科目:高中化学 来源:2011年普通高等学校招生全国统一考试化学卷(重庆) 题型:填空题
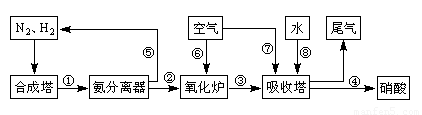
(16分)工业合成氨与制备硝酸一般可连续生产,流程如下:
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2。t℃时,往1L密闭容器中充入0.2mol
CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
CO2+H2。t℃时,往1L密闭容器中充入0.2mol
CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g) △H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。
2NH3(g) △H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。
|
T/℃ |
T1 |
300 |
T2 |
|
K |
1.00×107 |
2.45×105 |
1.88×103 |
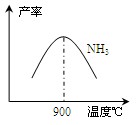
(3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示。温度高于900℃时,NH3产率下降的原因 。
(4)在上述流程图中,氧化炉中发生反应的化学方程式为
__________ _。
(5)硝酸厂的尾气直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H= -1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:________________________ 。
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式____________________,科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极是__________(填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
 (08福州市期末)已知反应N2(g)+3 H2(g) 2NH3(g),△H<0,向某体积恒定的密闭容器中按体积比l∶3充入N2和H2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图,Y可以是()
(08福州市期末)已知反应N2(g)+3 H2(g) 2NH3(g),△H<0,向某体积恒定的密闭容器中按体积比l∶3充入N2和H2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图,Y可以是()
A.N2的转化率 B.混合气体的密度
C.密闭容器的压强 D.H2的体积分数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com