
分析 4.8g A的物质的量为$\frac{4.8g}{60g/mol}$=0.08mol,与氧气在密闭容器中完全燃烧生成二氧化碳和水蒸气.将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.88g,为水的质量,且n(H2O)=$\frac{2.88g}{18g/mol}$=0.16mol,碱石灰增重7.04g,为二氧化碳的质量,且n(CO2)=$\frac{7.04g}{44g/mol}$=0.16mol,以此可确定有机物含有O的个数,可确定分子式,以此解答该题.
解答 解:(1)4.8g A与氧气在密闭容器中完全燃烧生成二氧化碳和水蒸气.将反应生成的气体依次通过浓硫酸和碱石灰,
浓硫酸增重2.88g,为水的质量,且n(H2O)=$\frac{2.88g}{18g/mol}$=0.16mol,n(H)=0.32mol,m(H)=0.32g,
碱石灰增重7.04g,为二氧化碳的质量,且n(CO2)=$\frac{7.04g}{44g/mol}$=0.16mol,n(C)=0.16mol,m(C)=0.16mol×12g/mol=1.92g,
则m(O)=4.8g-0.32g-1.92g=2.56g,
n(O)=$\frac{2.56g}{16g/mol}$=0.16mol,
故答案为:0.16;
(2)4.8g A的物质的量为$\frac{4.8g}{60g/mol}$=0.08mol,n(H)=0.32mol,n(C)=0.16mol,n(O)=0.16mol,则N(C)=$\frac{0.16mol}{0.08mol}$=2,N(H)=$\frac{0.32mol}{0.08mol}$=4,N(O)=$\frac{0.16mol}{0.08mol}$=2,
所以分子式为C2H4O2,
故答案为:C2H4O2.
点评 本题考查了有机物分子式的确定,为高频考点,题目难度中等,注意掌握质量守恒在确定有机物分子式中的应用方法,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
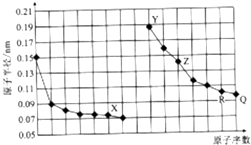
| A. | QX2、RX2都有杀菌消毒的作用,二者常用于自来水消毒 | |
| B. | 简单离子的半径:X>Y>Z | |
| C. | Y、Z、R对应的最高氧化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 复合材料一定是由两种或两种以上材料制成的 | |
| B. | 复合材料既保持了原材料的优点,又有优于原材料的特点 | |
| C. | 在复合材料中,增强体起骨架作用 | |
| D. | 传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其它分散系的本质特征是胶体可以发生丁达尔现象 | |
| B. | Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 | |
| C. | 用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同 | |
| D. | 硫酸的电离方程式为:H2SO4═2H++SO42- 点燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔融不导电 | B. | 水溶液不导电 | ||
| C. | 熔点比BeBr2高 | D. | 不与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乳酸CH3-CHOH-COOH | |
| B. | 甘油 CH2OH-CHOH-CH2OH | |
| C. | 脱氧核糖 CH2OH-CHOH-CHOH-CH2-CHO | |
| D. | 核糖 CH2OH-CHOH-CHOH-CHOH-CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在周期表中,元素的族序数都等于其原子的最外层电子数 | |
| B. | ⅦA族元素的单质,随分子量的增大,熔、沸点升高;ⅠA族单质,随分子量的增大,熔、沸点下降 | |
| C. | 周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强 | |
| D. | 同主族元素随原子核电荷数的递增,原子半径依次增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com