
下列反应的离子方程式正确的是
A. 用小苏打(NaHCO3)治疗胃酸(HCl)过多:CO32-+2H+ =CO2↑+H2O
B. 氯化铁溶液腐蚀铜箔制印刷线路板:Fe3++Cu=Fe2++ Cu2+
C. 氢氧化镁溶于盐酸:Mg(OH)2+2H+= Mg2++2H2O
D. Fe3+与I-反应的离子方程式为:Fe3++2I-= Fe2++ I2
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一下学期期初化学试卷(解析版) 题型:选择题
下列各组离子,能在溶液中大量共存的是
A. Na+ 、Mg2+ 、Cl- 、SO42- B. Na+ 、Ca2+ 、CO32- 、NO3-
C. Na+ 、H+ 、Cl- 、CO32- D. K+ 、Al3+ 、SO42- 、OH-
查看答案和解析>>
科目:高中化学 来源:河北省2016-2017学年高一下学期开学考试化学试卷 题型:选择题
设阿伏加德罗常数为NA,下列说法正确的是
A. 常温常压下,22.4LH2O中含有的氢原子数为2NA
B. 17gNH3与18 g H2O所含有电子数均为10NA
C. 2.7 g Al与足量的NaOH溶液反应,生成H2的分子数为0.1NA
D. 1 mol HCl气体中的分子数与2L 0.5 mol/L盐酸中的溶质粒子数相等
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一下学期开学考试化学试卷(解析版) 题型:计算题
按要求填空:
(1)0.2molO3和0.3molO2的质量___________(选填“相等”、“不相等”或“无法判断”),分子数之比为__________,所含原子数之比为___________,在相同条件下的体积之比为_____________。
(2)73gHCl气体中含有_____________个分子,标准状况下占有的体积为_____________L。
(3)相同物质的量浓度的KCl、MgCl2、AlCl3三种溶液,分别与AgNO3溶液反应,当生成的AgCl的沉淀的质量之比为3:2:1时,三种溶液的体积比为__________。
(4)标准状况下VL氯化氢气体溶解在1L水中,所得溶液的密度为ρg•mL,溶液中溶质的质量分数为ω,物质的量浓度为cmol•L-1,则ω=__________(任写一种表达式)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列有关实验的操作正确的是
实验 | 操作 | |
A | 配制稀硫酸 | 先将浓硫酸加入烧杯中,后倒入蒸馏水 |
B | 排水法收集KMnO4分解产生的O2 | 先熄灭酒精灯,后移出导管 |
C | 浓盐酸与MnO2反应制备纯净Cl2 | 气体产物先通过浓硫酸,后通过饱和食盐水 |
D | CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列实验操作与安全事故处理错误的是
A. 使用水银温度计测量烧杯中的水的温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中
B. 试管夹从试管底由下往上夹住试管口约 处,手持试管夹长柄末端进行加热
处,手持试管夹长柄末端进行加热
C. 燃着的酒精灯翻倒,酒精洒到桌面并且燃烧,为了人身安全,应立即撤离现场
D. 将玻璃管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻璃管插入端并缓慢旋进塞孔中
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团农二师华山中学高一下学期学前考试化学试卷(解析版) 题型:选择题
已知三个氧化还原反应:
①2FeCl3+2KI=2FeC12+2KCl+I2 ②2FeCl2+Cl2 =2FeCl3
③2KMnO4+16HCI(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
若某溶液中有Fe2+、I一、Cl—共存,要将I—氧化除去而不氧化Fe2+和Cl—,则可加入的试剂是
A. Cl2 B. KMnO4 C. FeCl3 D. HCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省广州市高一上学期期期末考试化学试卷(解析版) 题型:选择题
下列实验能达到预期目的的是
编号 | 实验内容 | 实验目的 |
A | 向某待测液中通入Cl2 ,再滴入2滴KSCN溶液后,溶液变为血红色 | 证明该待测液中一定含有Fe2+ |
B | 向某待测液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 证明该待测液中一定含有CO32- |
C | 把硫酸酸化的H2O2溶液滴入FeCl2溶液中,溶液变成黄色 | 证明H2O2氧化性大于Fe3+ |
D | 向Al(0H)3沉淀中分别加入盐酸和氨水,沉淀都会溶解 | 证明Al(0H)3是两性氢氧化物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:填空题
以NaCl等为原料制备KClO4的过程如下:
①在无隔膜、微酸性条件下,发生反应:NaCl+H2O—NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3。
③一定条件下反应:4KClO3=3KClO4+KCl,将产物分离得到KClO4。
(1)电解时,产生质量为2.13g NaClO3,同时得到H2的体积为____________L(标准状况)。
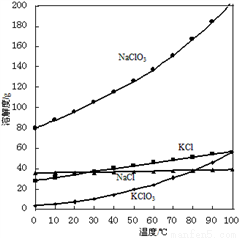
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是________________。
(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:
准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl- (反应为:3 KClO4 +C6H12O6 ═ 6 H2O + 6 CO2↑ + 3 KCl),加入少量K2CrO4溶液作指示剂,用0. 20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积21.00mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
① 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若c(CrO42-)=1.1×10-4mol/L,则此时c(Cl-)=________________mol/L。
② 计算KClO4样品的纯度(请写出计算过程。)______________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com