
| ����¯�¶�/�� | 600 | 620 | 640 | 660 |
| ¯����CuSO4����������/% | 9.3 | 9.2 | 9.0 | 8.4 |
���� ��1�����ݷ�Ӧ����������������غ�����д��ѧ����ʽ��
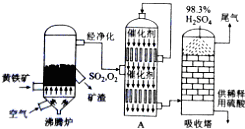
��2��SO2��O2�ķ�Ӧ�ڽӴ����н��У���ͼ��֪�����豸�ϲ�ѭ��ʹ�õ�������SO2��O2���²��Dz���SO3��
��3��SO3��H2O����ʱ�ų��������ȣ����γ�������������������������գ�
��4����һ����SO2����ȡ����Ҫԭ���ǻ�����Ϳ������ڸ��������գ�ʹ��Ԫ��ת���SO2���壬�豸Ϊ����¯����������Ҫ���飬������Ϳ����ĽӴ��棻�ڶ�����SO3����ȡ���ӷ���¯�г����������辭������������������Ӵ����ڴ���������SO2��O2��Ӧ����SO3���豸Ϊ�Ӵ��ң�ͬʱ�漰�����Ľ��������������á�ƽ����ƶ������⣻����������������ɣ��ӽӴ����г��������������������Ϊ���������γ�����ŨH2SO4���գ����Ṥҵβ���к����������ݶ�����������ʿ��ü�Һ���գ����Ṥҵ����Ӧ�����ۺϾ���Ч�����⣬ͬʱҪ���ǵ��ص���������������᳧��һ������һ����Ⱦ�ԵĹ�����
��5���ɱ������ݷ������¶Ⱥ�CuSO4����������֮��Ĺ�ϵ����CuSO4������ȡ����SO3 �����������ɷ�Ӧ2SO2��g��+O2��g�� $?_{��}^{����}$ 2SO3��g������H=-98.3kJ•mol-1����SO3 ���������¶�֮��Ĺ�ϵ��
��6��������������������Ӧ�����������������ᣬ�ݴ�д����Ӧ�����ӷ���ʽ������14H++Cr2O72-+6Fe2+�T2Cr3++6Fe3++7H2O��SO2+2Fe3++2H2O=SO42-+2Fe2++4H+��֪��3SO2��Cr2O72-������������ݽ��м��㣮
��� �⣺��1����Ӧ�����������֪����������غ�����д��ѧ����ʽΪ��4CuFeS2+13O2 $\frac{\underline{\;����\;}}{\;}$ 4CuO+2Fe2O3+8SO2���ʴ�Ϊ��4CuFeS2+13O2 $\frac{\underline{\;����\;}}{\;}$ 4CuO+2Fe2O3+8SO2��
��2��SO2��O2�ķ�Ӧ�ڽӴ����н��У���ͼ��֪�����豸�ϲ�ѭ��ʹ�õ�������SO2��O2���²��Dz���SO3��
�ʴ�Ϊ���Ӵ��ң�SO2��O2��
��3��SO3��H2O����ʱ�ų��������ȣ���ˮ��ϡ�����������γ����������������ڳɷ�����SO3������������������SO3����ˮ��ϡ���ᣬ��Ũ�������գ�
�ʴ�Ϊ�����Է�ֹ�γ�������ʹ��������������ȫ��
��4��A���ڷ���¯�У�ԭ�ϻ������ǹ��塢���������壬Ϊ�˼ӿ췴Ӧ���ʣ�����Ҫ����������飬����Ӵ��棬��߷�Ӧ���ʣ���A��ȷ��
B������¯�ų��Ŀ�����F2O3��F2O3�ɹ���������B��ȷ��
C������ֻ�ܸı䷴Ӧ���ʣ�����Ӱ��ת���ʣ���C����
D����ΪSO2+2NaOH�TNa2SO3+H2O������β����SO2����NaOHŨ��Һ�����գ���D��ȷ��
E�����Ṥҵ����Ӧ�����ۺϾ���Ч�����⣬ͬʱҪ���ǵ��ص���������������᳧��һ������һ����Ⱦ�ԵĹ������������᳧�ij�ַ��ѡ��������������Ĺ�ҵ���еĽ���
��E��ȷ��
�ʴ�Ϊ��ABDE��
��5�����᳧����¯�ų��Ŀ����к���Fe2O3��CuO��CuSO4����CuO��SO3 �ڷ���¯�л��϶��ɣ������������ɱ������ݿ�֪������ͭ���������������¯�¶����߶����ͣ�����Ϊ��ӦCuO+SO3 $\frac{\underline{\;����\;}}{\;}$ CuSO4��SO3���������ٵ��µģ�����2SO2��g��+O2��g��$?_{��}^{����}$ 2SO3��g����H=-98.3kJ•mol-1 ��Ӧ�Ʊ�SO3���÷�ӦΪ���淴Ӧ��������Ϊ���ȣ������¶����ߣ�ƽ�������ƶ�������SO3�������٣���CuO��SO3�ڷ���¯�л��϶���CuSO4����Ҳ���٣�
�ʴ�Ϊ��SO2ת��ΪSO3������Ӧ���ȵĿ��淴Ӧ�����¶����ߣ�ƽ�����ƣ�SO3���ʵ������٣�����CuSO4�������٣����¶����ߣ�SO3���ʵ������٣���CuSO4�������٣���
��6������14H++Cr2O72-+6Fe2+�T2Cr3++6Fe3++7H2O��SO2+2Fe3++2H2O=SO42-+2Fe2++4H+�ɵù�ϵʽ��
3SO2��Cr2O72-��
3 1
x 0.02mol/L��0.025L
��ã�x=$\frac{0.02mol/L��0.025L��3}{1}$=0.0015mol��
��Ӵ���������������SO2���������Ϊ��0.0015mol��$\frac{0.28L}{22.4L/mol}$��100%=12.00%��
�ʴ�Ϊ��12.00%��
���� ������ʵ�ʻ�����������ͭ����ۺ����á�Ϊ������������Ԫ�ػ�����֪ʶ�����ӷ���ʽ�ͻ�ѧ����ʽ����д����Ŀ��ע�ؿ���ѧ�����û�ѧԭ�������ʵ�������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ��������ľ̿���� | ||
| C�� | ��������ˮ | D�� | SO2��������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
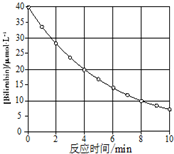 ������Bilirubin��һ�������Ĺ������·����ֽⷴӦ����Ӧ��Ũ���淴Ӧʱ��仯��ͼ��ʾ�����㷴Ӧ4��8min���ƽ����Ӧ���ʺ��Ʋ��16min��Ӧ���Ũ�ȣ����Ӧ�ǣ�������
������Bilirubin��һ�������Ĺ������·����ֽⷴӦ����Ӧ��Ũ���淴Ӧʱ��仯��ͼ��ʾ�����㷴Ӧ4��8min���ƽ����Ӧ���ʺ��Ʋ��16min��Ӧ���Ũ�ȣ����Ӧ�ǣ�������| A�� | 2.5 ��mol•L-1•min-1 ��2.0 ��mol•L-1•min-1 | |
| B�� | 2.5 ��mol•L-1•min-1 ��2.5 ��mol•L-1•min-1 | |
| C�� | 3.0 ��mol•L-1•min-1 ��3.0 ��mol•L-1•min-1 | |
| D�� | 5.0 ��mol•L-1•min-1 ��3.0 ��mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ɫ���ٱ仯 | B�� | ��������ܶȲ��ٱ仯 | ||
| C�� | 2v����N2O4��=v�棨NO2�� | D�� | ���������Է����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ȼ��ǰ��Ҫ���飬��Ϊ���IJ����ڿ���ȼ�� | |
| B�� | ����¯������¯���辻������Ϊ���е�SO2�������ʷ�Ӧ | |
| C�� | SO2����ΪSO3ʱ��ʹ�ô��������������IJ��� | |
| D�� | SO3��98.3%��Ũ�������գ�Ŀ���Ƿ�ֹ�γ���������ʹSO3������ȫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
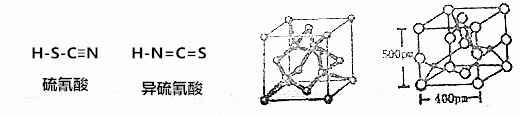
 Ԫ�����ڱ������кͷ�����Ԫ�ػ�̬ԭ�Ӻ�����ӵ��Ų�ϢϢ��أ���ݴ˻ش��������⣺
Ԫ�����ڱ������кͷ�����Ԫ�ػ�̬ԭ�Ӻ�����ӵ��Ų�ϢϢ��أ���ݴ˻ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
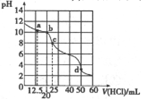 �����£���0.1000mol/L����ζ�25mL0.1000mol/LNa2A��Һ����֪H2AΪ��Ԫ���ᣩ����ζ�������ͼ��ʾ�����жԵζ���������Һ���������Ũ�ȹ�ϵ�ж���ȷ���ǣ�������
�����£���0.1000mol/L����ζ�25mL0.1000mol/LNa2A��Һ����֪H2AΪ��Ԫ���ᣩ����ζ�������ͼ��ʾ�����жԵζ���������Һ���������Ũ�ȹ�ϵ�ж���ȷ���ǣ�������| A�� | a�㣺c��A2-��=c��HA-�� | B�� | b�㣺5c��Cl-��=4[c��A2-��+c��HA-��+c��H2A��] | ||
| C�� | c�㣺c��Na+����c��HA-����c��A2-����c��H2A�� | D�� | d�㣺c��H+��=c��HA-��+c��A2-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{8}^{16}$O2-�Ľṹʾ��ͼ��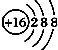 | |
| B�� | NH4Br�ĵ���ʽ��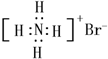 | |
| C�� | CCl4�Ľṹʽ 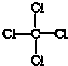 | |
| D�� | ��Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽ��1s22s12p3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com