
在一定条件下,下列药物的主要成分都能发生四种反应的是
①取代反应 ②加成反应 ③水解反应 ④中和
A.维生素B5: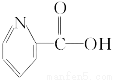
B.阿司匹林:
C.芬必得:
D.摇头丸:
科目:高中化学 来源: 题型:选择题
| A. | 35Cl2、37Cl2、35Cl、37Cl | B. | -OH、-CH2OH、-CH2CH2OH | ||
| C. | CH4、CH3CH(CH3)2、(CH3)3CCH2CH3 | D. | 一氯甲烷、二氯甲烷、三氯甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三月考二化学试卷(解析版) 题型:选择题
下列说法正确的是
A.甲烷、汽油、生物柴油、酒精都是碳氢化合物,都可作燃料
B.可食用植物油含有的高级脂肪酸甘油酯是人体的营养物质
C.钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高
D.用CuSO4溶液使蛋清溶液发生盐析,进而提纯分离蛋白质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学试卷(解析版) 题型:选择题
下表是食用碘盐包装上的部分说明,下列说法正确的是
配料 | 精盐、碘酸钾、抗结剂 |
碘含量 | 35±15 mg·kg-1 |
储存方法 | 密封、避光、防潮 |
食用方法 | 烹饪时,待食品熟后加入碘盐 |
A. 高温会导致碘的损失
高温会导致碘的损失
B.碘酸钾可氧化氯化钠
C.可用淀粉检验碘盐中的碘酸钾
D.该碘盐中碘酸钾含量为20~50 mg·kg-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:实验题
(1)甲:量取20ml 18mol/L浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100ml容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①实验所用的玻璃仪器除烧杯和容量瓶外,还有??????????______________
②将溶液转移到容量瓶中的正确操作是??????????______________;
(2)乙:用100ml 量筒量取20ml 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100ml 刻度线,再搅拌均匀.
你认为此法是否正确?若不正确,指出其中错误之处??????????______________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是
A.由已知信息可得:NA= B.Wg该原子的物质的量一定是
B.Wg该原子的物质的量一定是  mol
mol
C.Wg该原子中含有 个该原子g D.该原子的摩尔质量是aNA g
个该原子g D.该原子的摩尔质量是aNA g
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com