
| A. | 锗的第一电离能高于碳而电负性低于碳 | |
| B. | 四氯化锗与四氯化碳分子都是四面体构型 | |
| C. | 二氧化锗与二氧化碳都是非极性的气体化合物 | |
| D. | 锗和碳都存在具有原子晶体结构的单质 |
分析 A.非金属性越强,第一电离能越大;
B.四氯化锗与四氯化碳分子中,中心原子均为sp3杂化;
C.二氧化锗为离子化合物,二氧化碳为共价化合物;
D.锗和碳都易于形成四个键,能形成空间网状结构.
解答 解:A.碳和锗同主族,碳在第二周期,而锗在第四周期,锗是金属元素,碳的非金属性强,故锗的第一电离能低于碳,故A错误;
B.四氯化锗和四氯化碳都是分子晶体且构型相同,中心原子均为sp3杂化,均是正四面体结构,故B正确;
C.金属的氧化物为固体,即二氧化锗不是气体,二氧化碳都是非极性的气体化合物,故C错误;
D.锗和碳都易于形成四个键,能形成空间网状结构,能形成原子晶体结构的单质,故D正确;
故选BD.
点评 本题考查元素周期表及元素周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意选项BD为解答的难点,题目难度不大.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:多选题
| A. | 若pH=7,HA的浓度一定为0.1 mol•L-1 | |
| B. | 若pH>7,HA的pH不可能等于1 | |
| C. | 若pH<7,溶液中的微粒浓度关系为:c(Na+)=c(HA)+c(A-) | |
| D. | 若pH=12,且HA为强酸时,HA的浓度应为0.08 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入AgNO3溶液,有白色沉淀产生 | |
| B. | 加入稀盐酸溶液,无明显现象,再加入BaCl2溶液,产生白色沉淀 | |
| C. | 加入Ba(NO3)2溶液,产生白色沉淀,再加入稀盐酸,沉淀不溶解 | |
| D. | 加入BaCl2溶液,产生白色沉淀,再加入稀盐酸,沉淀不溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

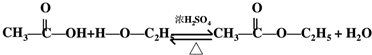 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
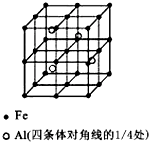 一种Al-Fe合金的立体晶胞结构如图,请据此回答下列问题:
一种Al-Fe合金的立体晶胞结构如图,请据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | C的物质的量浓度 | D. | 气体的总物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2A+3B?2C | B. | 2A+3B?3C | C. | 3A+2B?3C | D. | 3A+2B?2C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 124gP4中含P-P键的数目为4NA | B. | 60gSiO2中含有Si-O键的数目为2NA | ||
| C. | 12g石墨中含C-C键的数目为1.5NA | D. | 12g金刚石中含C-C键的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
| A. | KBr | B. | KI | C. | K2S | D. | K2CrO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com