
已知A、B、C、D、E、F、G、H、I是中学化学中常见的九种化合物,其中B常温下为无色无味透明的液体,C焰色反应火焰呈黄色,E是红棕色的固体;X、Y是两种常见的单质,其中X常温常压下为气体。
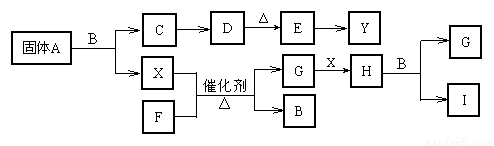
根据上面框图关系填空。
(1)A的化学式为________________,固体A的颜色为__________________;
(2)写出“X+F G+B”的化学反应方程式________________________;
G+B”的化学反应方程式________________________;
(3)写出“实验室中制取F气体”的化学反应方程式_____________________;
(4)写出“C→D”反应的离子方程式_________________________;
(5)写出“E+金属单质 Y+两性氧化物”的化学反应方程式___________________。
Y+两性氧化物”的化学反应方程式___________________。
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源:2017届山东省高三上10月模块测试化学试卷(解析版) 题型:选择题
除去下列物质中的杂质选用的试剂和方法最合理的是( )
物质 | 杂质 | 试剂 | 方法 | |
A | 二氧化碳 | 二氧化硫 | NaOH溶液 | 洗气 |
B | 氯化亚铁溶液 | 氯化铁 | 过量铁粉 | 过滤 |
C | 氧化铁 | 氧化铝 | 氨水 | 过滤 |
D | 氯化钠溶液 | 碘化钠 | 四氯化 | 萃取 |
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三上统一考试化学试卷(解析版) 题型:选择题
已知NH4CuSO3与足量的10mol/L硫酸液混合微热,产生下列现象:
①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色.
据此判断下列说法正确的是( )
A.反应中硫酸作氧化剂
B.NH4CuSO3中硫元素被氧化
C.刺激性气味的气体是氨气
D.1mol NH4CuSO3完全反应转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源:2017届江西省赣州市十四校高三上期中联考化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | L | M | X | R | T |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
下列叙述正确的是( )
A.离子半径大小:r(M3+)>r(T2-)
B.R的氧化物对应的水化物可能具有两性
C.X单质在氧气中燃烧生成XO3
D.L、X形成的简单离子核外电子数不相等
查看答案和解析>>
科目:高中化学 来源:2017届江西省赣州市十四校高三上期中联考化学试卷(解析版) 题型:选择题
我国古代有“银针验毒”的记载。“银针验毒”的反应原理之一是4Ag+2H2S+O2=2X+2H2O。下列有关该反应的说法正确的是( )
A.Ag得到电子 B.X为AgS
C.O2被还原 D.每生成1 mo1X转移电子数4NA
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省六校协作体高三上学期期中化学试卷(解析版) 题型:选择题
有甲、乙、丙、丁四种易溶于水的物质,分别由以下离子(NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-)中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论正确的是
A.甲为氯化钡 B.乙溶液含有Cl-
C.丙溶液含有 SO42- D.丁溶液含有NH4+
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省六校协作体高三上学期期中化学试卷(解析版) 题型:选择题
关于某溶液中所含离子的鉴别,下列判断正确的是
A.加入BaCl2溶液,生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含有SO42-
B.加入NaOH溶液,生成的白色沉淀在空气中迅速变为灰绿色,最终变为红褐色,则原溶液中一定含有Fe2+。
C.用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含有K+
D.加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三10月月考化学卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是(  )
)
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
B.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+
C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
查看答案和解析>>
科目:高中化学 来源:2017届四川省资阳市高三上第一次诊断化学试卷(解析版) 题型:实验题
废旧显示屏玻璃中含有SiO2、Fe2O3、CeO2、FeO等物质。某课题小组以此玻璃粉末为原料,制得Ce(OH)4和硫酸铁铵矾[化学式为xFe2(SO4)3·y(NH4)2SO4·zH2O],流程设计如下:
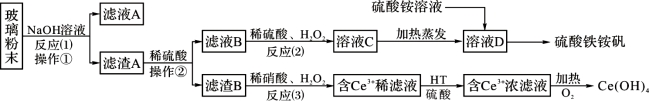
已知:Ⅰ、酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式,Ce4+有较强氧化性;
Ⅱ、CeO2不溶于稀硫酸,也不溶于氢氧化钠溶液。
回答以下问题:
(1)操作①的名称是_____________;该操作所用的玻璃仪器有:烧杯、_________、_________。
(2)反应(2)中过氧化氢的作用是:_________________________。
(3)反应(3)的离子方程式是:_____________________。
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:
2Ce3+(水层)+6HT(有机层) 2CeT3(有机层)+6H+(水层)
2CeT3(有机层)+6H+(水层)
从平衡角度解释:向CeT3(有机层)加入硫酸获得较纯的含Ce3+的水溶液的原因是_________________。
(5)硫酸铁铵矾广泛用于水的净化处理,其净水原理用离子方程式表示为:_________________。
(6)相同物质的量浓度的以下四种溶液中,铵根离子浓度由大到小的顺序是:_________________。
a.xFe2(SO4)3·y(NH4)2SO4·zH2O
b.(NH4)2SO4
c.(NH4)2CO3
d.NH3·H2O
(7)为测定某硫酸铁铵矾样品的组成,现称取14.00 g该样品,将其溶于水配制成100 mL溶液;再将溶液分成两等份,向其中一份加入足量氢氧化钠溶液,过滤、洗涤沉淀、再烘干灼烧至恒重,得到1.60 g固体;向另一份溶液中加入0.5 mol/L硝酸钡溶液100 mL,恰好完全反应。则该硫酸铁铵矾的化学式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com