
| A、v(NH3)=0.001mol?L-1?s-1 |
| B、v(H2O)=0.001mol?L-1?s-1 |
| C、v(NO)=0.09mol?L-1?s-1 |
| D、v(O2)=0.05mol?L-1?s-1 |
| ||
| △t |
| ||
| 30s |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 5 |
| 6 |
| 5 |
| 6 |


科目:高中化学 来源: 题型:
| A、雨水样品酸度逐渐减小 |
| B、雨水样品酸度没变化 |
| C、雨水样品继续吸收空气中的CO2 |
| D、雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe和FeCl3 |
| B、Na与O2 |
| C、NaOH与CO2 |
| D、NaOH与AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界硅的贮量丰富 |
| B、自然界中存在大量单质硅 |
| C、高纯度的二氧化硅被用于制作计算机芯片 |
| D、光导纤维的主要成分是Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
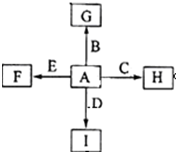 如图中,A、D、是常见非金属单质B、C、E是常见金属单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知
如图中,A、D、是常见非金属单质B、C、E是常见金属单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com