
关于化学键的下列叙述中,正确的是
| A.离子化合物不可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.共价化合物中不含离子键 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
NH3分子空间构型是三角锥形,而CH4是正四面体形,这是因为
| A.NH3分子中N为sp2杂化,CH4分子中C为sp3杂化 |
| B.NH3分子中N原子形成3个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.中心原子N、C都是sp3杂化,但NH3分子中N原子上的一未形成共价键的孤对电子对分子构型有影响,CH4分子中共价键完全相同且分子构型完全对称 |
| D.NH3分子中3个N—H键长大于CH4分子中4个C—H键长 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列变化中,既有共价键和离子键断裂,又有共价键和离子键形成的是
| A.2Na2O2+2CO2=2Na2CO3+O2 | B.2Na+2H2O=2NaOH+H2↑ |
| C.Cl2+H2O?=?HCl+HclO | D.Na2CO3+BaCl2=BaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
按要求回答下列问题:
(1)有下列六种物质:①碳60(C60)晶体②硼晶体③Na2O晶体④ CaF2晶体⑤P4O10晶体⑥碳化硅晶体。其中属于离子晶体的是 ,属于分子晶体的是 ,属于原子晶体的是____。
(2)有下列分子:HCN、P4、SO3、PCl3、BF3,其中属于非极性分子的是 。
(3)有下列离子:SO32-、SO42-、CO32-,其中VSEPR模型为正四面体形的是 ,中心原子的杂化轨道类型属于sp2杂化的是 。
(4)CaO晶胞如右图所示,CaO晶体中Ca2+的配位数为______;与每一个钙离子距离最近并且距离相等的钙离子有____个 ;CaO晶体和NaCl晶体的晶格能分别为:CaO:3 401 kJ/mol、NaCl:786 kJ/mol。导致两者晶格能差异的主要原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
研究人员最近发现,在一定的实验条件下,给水施加一个弱电场,在20℃、1个大气压下,水可以结成冰,称为“热冰”。图Ⅰ是水和“热冰”的计算机模拟图,图中球代表水分子中的原子。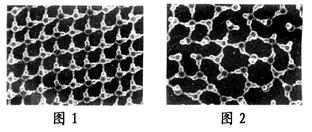
图Ⅰ
(1)图中较大的球代表________原子,其原子结构示意图是________。水分子中氢氧原子间的化学键是________(填“共价键”或“离子键”)。
(2)用球棍模型表示的水分子结构是________。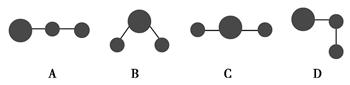
图Ⅱ
(3)已知水分子中氧原子一端带部分负电荷,氢原子一端带部分正电荷,在外加电场作用下,水结成冰。图Ⅰ中模拟“热冰”的示意图是________(填“图1”或“图2”),理由是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有H、C、O、Cl、Na五种元素。
(1)在由两种元素组成的化合物里,其中离子化合物有(写2种)______________________,共价化合物有(写2种)______________________。
(2)在由三种元素组成的化合物里,其中离子化合物有(写2种)______________________,共价化合物有(写2种)______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关粒子间的作用力,说法正确的是
| A.HCI溶于水时.H— Cl键会断裂 |
| B.H2O2分子中只有极性键 |
| C.NH3是以非极性键结合的分子 |
| D.MgCl2中既有离子键,又有共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com