
| A. | a=10、b=9.2 | B. | a<10、b>9.2 | C. | a>10、b=9.2 | D. | a>10、b<9.2 |
分析 根据稀释过程中溶质硫酸的质量不变列方程计算加入水的体积a,结合c=$\frac{1000ρω}{M}$mol/L判断49%的硫酸的浓度,注意硫酸的浓度越大,其密度越大.
解答 解:稀释过程中溶质硫酸的质量不变,则:10mL×1.84g/mL×98%=(10mL×1.84g/mL+amL×1g/mL)×49%,解得a=18.4>10;
设49%的硫酸的密度为ρg/mL,硫酸的浓度越大密度越大,则ρ<1.84,49%的硫酸的物质的量浓度b=$\frac{1000ρ×49%}{98}$mol/L=5ρ mol/L<9.2mol/L,
故选D.
点评 本题考查溶液浓度的有关计算,题目难度中等,注意掌握物质的量浓度与质量分数之间的关系,明确硫酸的浓度越大密度越大为解答关键.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,若D最外层只有两个电子,则D的原子结构示意图
,若D最外层只有两个电子,则D的原子结构示意图 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5+3-3 | -2 |
| A. | X.Y元素的金属性:X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物的水化物能溶于稀氨水 | |
| D. | Z的最高价氧化物的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
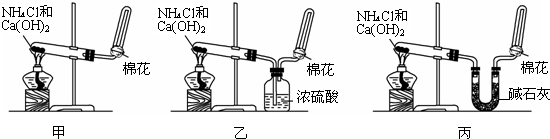
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com