
����Ŀ������Ԫ�صĻ��ϼ��Ʋ����ʵ������ǻ�ѧ�о�����Ҫ�ֶΣ���ͼ����Ԫ�صij������ϼ��벿���������Ķ�Ӧ��ϵ��
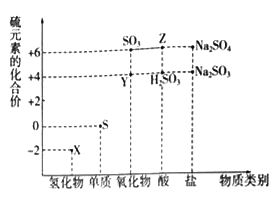
��1������Ԫ�ػ��ϼ۱仯�ĽǶȷ�����ͼ�м������������л�ԭ�ԵĻ�������_______���ѧʽ����
��2����X��Y��ϣ������ɵ���ɫ���壮�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_______��
��3����������Y�ķ�����_______________________________��
��4��Z��Ũ��Һ��ͭ������һ�������¿��Է�����ѧ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ_______��
��5��Na2S2O3����Ҫ�Ļ���ԭ�ϣ���������ԭ��Ӧ�ĽǶȷ����������Ʊ�Na2S2O3�ķ��������Ͽ��е���______������ţ���
a��Na2S+S b��Na2SO3+S c��SO2+Na2SO4 d��Na2SO3+Na2SO4
��6����֪Na2SO3�ܱ�K2Cr207����ΪNa2SO4��24mL 0.05molL��1��Na2SO3��Һ�� 20mL 0.02molL��1����Һǡ�÷�Ӧʱ��CrԪ���ڻ�ԭ�����еĻ��ϼ�Ϊ________��
���𰸡� SO2��H2SO3��Na2SO3 1��2 ��Yͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ�����Ⱥ��ֱ��ɫ Cu+2H2SO4��Ũ��![]() CuSO4+2H2O+SO2�� b +3
CuSO4+2H2O+SO2�� b +3
��������SԪ�صĻ��ϼ��Щ�2�ۡ�0�ۡ�+4�ۡ�+6�ۣ�
��1�������м��̬��Ԫ�ؼ��л�ԭ�����������ԣ�SԪ�صĻ��ϼ��Щ�2�ۡ�0�ۡ�+4�ۡ�+6�ۣ�����0�ۺ�+4��S�Ļ�������л�ԭ�����������ԣ���SO2��H2SO3��Na2SO3��
��2����XΪH2S��SO2��ϣ������ɵ���ɫ���壬���ö�������������������������ɵ���ɫ����S��ˮ��2H2S+SO2=3S��+2H2O����Ӧ����Ԫ�ػ��ϼ۩�2�۱仯Ϊ0�ۣ�H2S����ԭ����+4�۱仯Ϊ0�ۣ���������������������÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��2��
��3�������������Ư���Կ���ʹƷ����Һ��ɫ�������ֻ�ָ���ɫ�������Y�ķ����ǣ���Yͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ�����Ⱥ��ֱ��ɫ��
��4��Ũ������Һ��ͭ�����ڼ��������¿��Է�����ѧ��Ӧ��������ͭ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Cu+2H2SO4��Ũ��![]() CuSO4+2H2O+SO2����
CuSO4+2H2O+SO2����
��5��Na2S2O3��SΪ+2�ۣ���������ԭ�ĽǶȷ�������Ӧ����SԪ�ػ��ϼ۱���ֱ����2��С��2��a��S���ϼ۶�С��2��cd��S�Ļ��ϼ۶�����2��b����������
��6����CrԪ���ڲ����еĻ��ϼ�Ϊa�ۣ����ݵ���ת���غ㣬��24��10��3L��0.05mol/L����6��4��=20��10��3L��0.02mol/L��2����6��a�������a=+3 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�Ҵ��ͻ�����������ը���д�����Cl2��ɢ������Ӧ����ʩ����ȷ����
A����˳�緽��ĵ��ݴ���
B���ý��д���Һ��ë����ס�ڱ�Ѹ������
C������緽��ĸߴ���
D������������Ŀ��ý�ʪ���ޱ��º��Ŵ�������ʱ�����Ԯ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ�������й�������ȷ���ǣ�������
A. l mol OH������������Ϊ10NA
B. 2L0.5 molL��1Na2SO4��Һ�����������������Ϊ0.2NA
C. ��״���£�1.12 L CC14���е���ԭ����Ϊ0.2NA
D. 14 g��CO��N2��ɵĻ�������к��еķ�������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1molL��1ijһԪ�ᣨHA����Һ�� ![]() =1��10��8 �� ��ͬ���ʵ���Ũ�ȵ�ijһԪ�BOH����Һ��
=1��10��8 �� ��ͬ���ʵ���Ũ�ȵ�ijһԪ�BOH����Һ�� ![]() =1��1012 �� ����������ȷ���ǣ� ��
=1��1012 �� ����������ȷ���ǣ� ��
A.HA��pH=3��BOH��pH=13
B.pH=a��HA��Һ��ϡ��10������pH=a+1
C.�������HA��BOHǡ����ȫ��Ӧ����Һ��pH=7
D.��ͬ�����ͬpH��HA������ֱ�������Zn��Ӧ���������������ʵ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����������ȷ����
A.1��2���������� B.3��������
C.4�������� D.2���һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨ�Ҵ��Ľṹʽ�������������ˮ�ƾ����Ʒ�Ӧ��ʵ��װ�úͲⶨ��������IJ���װ�ã�
��1���ر�ͼAװ���е�ֹˮ��a����������b��Һ�����µΣ�ֱ��ȫ��������ƿ�����ж�Bװ���Ƿ�©�����©��������©��������ȷ��������ԭ�� ��
��2��װ��B�ж���ʱӦ��ʹ ��
��3��ʵ��ǰԤ�Ƚ�С�����ڶ��ױ����ڻ���С���飬��ȴ������ƿ�У���Ŀ���� ��
��4���������ʵ�������������״���µ����ݣ���ˮ�ƾ����ܶ�Ϊ�� gcm��3 �� VmL�ƾ���Ӧ��ȫ����Ͳ�ڵ�Һ�����Ϊm mL�����Ҵ��������ܱ���ȡ������ԭ�����ɱ�ʾΪ �� ���ú�������ĸ�Ĵ���ʽ��ʾ���ɣ�
��5����ʵ�����ⶨ�Ľ��ƫ�ߣ����������ԭ��������д��ţ����ٷ�Ӧ������̶���
����ˮ�ƾ��л��������״�
����ˮ�ƾ����Ƶķ�Ӧ������ȫ
����ˮ������װ�õ�������ˮ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������,����Һ�п��Դ����������( �� )
A. H+��Na+��NO3����OH��B. Na+��K+��NO3����Cl��
C. Ca2+��K+��AlO2����CO32��D. Ba2+��NH4+��HCO3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.��֬��������������л��߷��ӻ�����
B.�����ߡ����¡��ƾ���ɱ��������ԭ���ǵ����ʱ���
C.���ϡ��ϳ���ά���ϳ���Ϊ����ϳɸ߷��Ӳ���
D.ά����C�ֳƿ���Ѫ�ᣬ�����߲��и���ά����C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ѫ�쵰���к���Fe2+ �� �����ʳ�������Σ���ʹ���ж�����Ϊ�������λ�ʹFe2+ת���Fe3+ �� ���ɸ���Ѫ�쵰��ɥʧ��O2��ϵ�����������ά����C�ɻ����������ε��ж�����˵��ά����C���У�����
A.����
B.����
C.������
D.��ԭ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com