
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7;K2=5.6×10-11 |
下列选项错误的是
A.2CN-+H2O+CO2=2HCN+CO32- B.2HCOOH+CO32-=2HCOO-+H2O+CO2↑
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者等于后者
科目:高中化学 来源: 题型:
NA表示阿佛加德罗常数,下列说法正确的是
A.60克SiO2含有2NA个Si-O共价键
B.1.0 L 1.0 mo1/L的NaAlO2水溶液中含有的氧原子数为2NA
C.8.2 g Na218O2与足量的CO2和H2O(g)的混合气体充分反应后转移电子数为0.1NA
D.NA个Fe(OH)3胶体粒子的质量为107g
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① | ||||||||||||||||||
| ② | ③ | |||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | |||||||||||||||
| ⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)表中属于d区元素的是 (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见
溶剂的化学式为 ,其立体构型为________________。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与
元素①所形成化合物的水溶液显 性(填“酸”或“碱”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑦和⑧形成的化合物的电子式为 。
(6)元素⑩的基态原子核外电子排布式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:① CH3COOH与CH3COONa等物质的量混合配成的稀溶液,pH为4.7;
② 用等物质的量的HCN和NaCN配成的稀溶液中,C(CN-)<C(Na+)。
则下列说法不正确的是
A. CH3COONa的水解趋势大于CH3COOH的电离趋势
B. NaCN的水解趋势大于HCN的电离趋势
C. ②溶液中,c(H+)<c(OH-)
D. CH3COONa的存在抑制了CH3COOH的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,最好依次通过盛有什么试剂的洗气瓶
A.澄清石灰水、浓H2SO4 B.KMnO4酸 性溶液、浓H2SO4
性溶液、浓H2SO4
C.溴水、浓H2SO4 D.浓H2SO4、KMnO4酸性溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)= 1.8×10-10,Ksp(AgY)= 1.0×10-12,Ksp(AgZ)= 8.7×10-17;
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1L溶液)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-) (填“增大”、“减小”或“不变”)。
(3)在25℃时,若取0.188g的AgY(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中c(Y-)= mol/L
(4)①由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:
② 在上述(3)的体系中,能否实现AgY向AgX的转化?
请通过计算,简述能否实现转化的理由是:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在生产、生活和科技等方面的叙述不正确的是( )
A.生铁、普通钢和不锈钢中的碳含量依次增加
B.硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂
C.节日燃放的烟花是某些金属元素发生焰色反应所呈现出来的色彩
D.明矾在自然水中生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生为探究钠与CO2的反应,利用如下装置进行实验。(已知PdCl2能被CO还原得到黑色的Pd)。可供选择的药品有:CaCO3(块状)、Na2CO3(粉末)、盐酸、稀硫酸、钠。
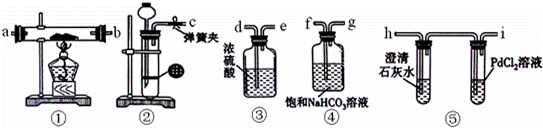
(1)请将上图各装置连接完整:②→ → →①→ 。(填装置序号)
(2)装置②有孔塑料板上所放的药品是: 。
(3)检查装置气密性并装好药品后,当观察到 现象时才点燃酒精灯,此步骤操作的目的是 。
(4)已知CO在潮湿环境中可将PdCl2还原为黑色粉末状的钯(Pd),写出该反应的化学方程式 。
(5)实验过程中CO2足量,装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。据此现象写出Na与CO2反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应中,不属于四种基本反 应类型的是( )。
应类型的是( )。
A.2FeCl3+Cu=2FeCl2+CuCl2 B.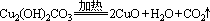
C.4Fe(OH)2+O2+2H2O= 4Fe(OH)3 D.CaCO3+2HCl=CaCl2+H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com