
| A. | 18.75% | B. | 30% | C. | 15% | D. | 22.5% |
分析 丁烷结构简式为:CH3-CH2-CH2-CH3,断键位置只有两种, ,故可生成甲烷、丙烯、乙烷、乙烯四种物质,设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,裂化生成的两种烯烃物质的量相等,则x=y,根据各个物理量之间的关系式列方程组计算.
,故可生成甲烷、丙烯、乙烷、乙烯四种物质,设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,裂化生成的两种烯烃物质的量相等,则x=y,根据各个物理量之间的关系式列方程组计算.
解答 解:丁烷结构简式为:CH3-CH2-CH2-CH3,断键位置只有两种, ,故可生成甲烷、丙烯、乙烷、乙烯四种物质,设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,裂化生成的两种烯烃物质的量相等,则x=y,
,故可生成甲烷、丙烯、乙烷、乙烯四种物质,设丁烷的物质的量为1mol,裂解成CH4和C3H6为xmol,裂解成C2H6和C2H4为ymol,裂化生成的两种烯烃物质的量相等,则x=y,
则$\left\{\begin{array}{l}{x+y=1×60%}\\{x=y}\end{array}\right.$,$\left\{\begin{array}{l}{x=0.3}\\{y=0.3}\end{array}\right.$,
含氢质量分数最高的是甲烷,其物质的量为0.3mol,因为是相同条件下,气体摩尔体积相同,甲烷的物质的量分数就等于甲烷占混合气体的体积分数=$\frac{0.3mol}{0.3mol×4+1mol×(1-60%)}×100%$=18.75%,故选A.
点评 本题考查化学方程式有关计算,为高频考点,侧重考查学生分析计算能力,明确烷烃裂解原理是解本题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
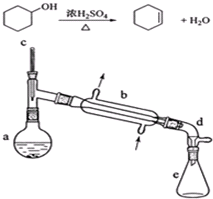
| 相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极反应式为O2+4e-═2O2- | |
| B. | 放电时溶液中的阳离子向正极方向移动 | |
| C. | 该电池反应为CH4+2O2═CO2+2H2O | |
| D. | 通入CH4一极的电极反应式为CH4+2O2+8e-═CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4gCu在足量的硫蒸气中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,11.2LSO2和SO3的混合物中硫原子数为0.5NA | |
| C. | 1L0.1mol•L-1的NH4Cl溶液中NH4+数目为0.1NA | |
| D. | 通常情况下,3.4gNH3中共用电子对数为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液(FeCl3):加入过量Cu后过滤 | |
| B. | Na2CO3固体(NaHCO3):加热 | |
| C. | CH3COOCH2CH3(CH3COOH):加NaOH溶液后振荡、分液 | |
| D. | Cl2(HCl):通过NaOH溶液后干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
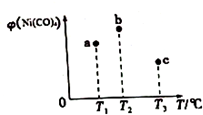 在容积均为1L的三个密闭容器中,分别放入镍粉并充入1molCO,控制作在不同温度下发生反应:Ni(s)+4CO(g)?Ni(CO)4(g),当反应进行到5min时,测得Ni(CO)4的体积分数与温度的关系如图所示.下列说法正确的是( )
在容积均为1L的三个密闭容器中,分别放入镍粉并充入1molCO,控制作在不同温度下发生反应:Ni(s)+4CO(g)?Ni(CO)4(g),当反应进行到5min时,测得Ni(CO)4的体积分数与温度的关系如图所示.下列说法正确的是( )| A. | 正反应为吸热反应,平衡常数:K(T1)>K(T2) | |
| B. | 反应进行到5min时,b容器中v(正)=v(逆) | |
| C. | 达到平衡时,a、b、c中CO的转化率为b>a>c | |
| D. | 减压或升温可将b中的平衡状态转变成c中的平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 300 | 727 | 1 227 |
| lg K | 6.17 | 2.87 | 1.24 |
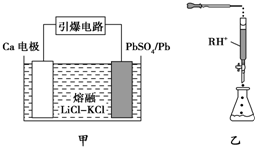
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com