
分析 (1)1100℃时,若平衡向右进行,CO物质的量减小、CO2物质的量增大;
(2).计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行,进而判断V正、V逆相对大小.
解答 解:(1)1100℃时,若平衡向右进行,CO物质的量减小、CO2物质的量增大,则高炉内CO2和CO的体积比值增大,故答案为:增大;
(2)浓度商Qc=$\frac{0.025}{0.1}$=0.25<K=0.263,说明不是平衡状态,且向正反应方向进行,则V正>V逆相,
故答案为:否;大于;浓度商Qc=$\frac{0.025}{0.1}$=0.25<K=0.263,说明不是平衡状态,且向正反应方向进行.
点评 本题考查化学平衡计算及影响因素,涉及平衡常数应用,难度不大,理解根据浓度商与平衡常数相对大小判断反应进行方向.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 3Fe+4H2O═Fe3O4+4H2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | SnCl4+2H2O═SnO2+4HCl | D. | 2Na2O2+2CO2═2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
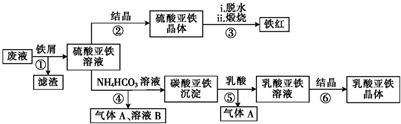
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.7 mol | B. | 0.9 mol | C. | 1.1 mol | D. | 1.3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知H2C2O4为二元弱酸,则Na2C2O4溶液:c (OH-)=c(H+)+c(HC2O4-)+c(H2C2O4) | |
| B. | 饱和碳酸钠溶液中:c(Na+)=2c(CO32-) | |
| C. | 饱和食盐水中:c(Na+)+c (OH-)=c(Cl-)+c(H+) | |
| D. | 50℃时,pH=12的NaOH溶液中:c(OH-)=1.0×10-2 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com