
回答下列问题。
(1)常温时,FeCl3 溶液的pH 7(填“>”、“<”或“=”),实验室配制FeCl3溶液时常将FeCl3固体先溶于较浓的盐酸溶液中,然后再用蒸馏水稀释到所需的浓度,原因是 ;将FeCl3溶液蒸干、灼烧,此过程中所涉及到的化学方程式是 。
(2)25℃时,向0.1 mol·L-1氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH减小,主要原因是 。
(3)某溶液中只存在OH-、H+、Na+、CH3COO-四种离子。
①若溶液中只溶解了一种溶质,该溶质的名称是 ,该溶液中四种离子的浓度由大到小的顺序为 。
②若溶液中四种离子的大小顺序为c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则溶液中溶质的化学式为 。
③若溶液中c(Na+)=c(CH3COO-),则该溶液显 (填“酸性”、“碱性”、“中性”),该溶液由体积相等的稀NaOH和CH3COOH溶液混合而成,则混合前c(NaOH) c(CH3COOH)(填“>”、“<”或“=”)。
(1)<,(1分) Fe3+发生水解,加入盐酸后,抑制其水解。(2分)
FeCl3+3H2O Fe(OH)3+3HCl 或FeCl3+3H2O
Fe(OH)3+3HCl 或FeCl3+3H2O Fe(OH)3↓+3HCl ↑( 2分
)
Fe(OH)3↓+3HCl ↑( 2分
)
2Fe(OH)3 Fe2O3+3H2O
(2分)
Fe2O3+3H2O
(2分)
(2)氨水中存在电离平衡NH3·H2O NH4+ + OH-。NH4Cl溶于水,发生电离NH4Cl=NH4++Cl-,产生大量NH4+,使氨水的电离平衡向左移动,溶液中c(OH-)减小。(3分)
NH4+ + OH-。NH4Cl溶于水,发生电离NH4Cl=NH4++Cl-,产生大量NH4+,使氨水的电离平衡向左移动,溶液中c(OH-)减小。(3分)
(3)① 醋酸钠 c(Na+)>c(CH3COO-)>c(OH-)>c(H+) (每空1分,共2)
②NaOH、CH3COONa (2分) ③中性,< (每空1分,共2分))
【解析】
试题分析:(1)氯化铁是强酸弱碱盐,溶于水铁离子水解溶液显酸性,因此常温时,FeCl3
溶液的pH<7;氯化铁是强酸弱碱盐,溶于水铁离子水解溶液显酸性,加入盐酸后,抑制铁离子水解;水解是吸热的,加热促进水解。且生成的氯化氢极易挥发,因此最终得到氢氧化铁固体,进一步灼烧得到氧化铁,反应的反应式有FeCl3+3H2O Fe(OH)3+3HCl或FeCl3+3H2O
Fe(OH)3+3HCl或FeCl3+3H2O Fe(OH)3↓+3HCl↑、2Fe(OH)3
Fe(OH)3↓+3HCl↑、2Fe(OH)3 Fe2O3+3H2O。
Fe2O3+3H2O。
(2)氨水中存在一水合氨的电离平衡NH3·H2O NH4+ + OH-。NH4Cl溶于水,发生电离NH4Cl=NH4++Cl-,产生大量NH4+,增大溶液中c(NH4+)浓度,使一水合氨的电离平衡向左移动,因此溶液中c(OH-)减小。
NH4+ + OH-。NH4Cl溶于水,发生电离NH4Cl=NH4++Cl-,产生大量NH4+,增大溶液中c(NH4+)浓度,使一水合氨的电离平衡向左移动,因此溶液中c(OH-)减小。
(3)①只有醋酸钠能同时电离出Na+、CH3COO-,而任何溶液中都存在水的电离平衡,所以若溶液中只溶解了一种溶质,该溶质的名称是醋酸钠。醋酸钠溶于水电离出的CH3COO-水解溶液显碱性,所以溶液中离子浓度大小关系是c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。
②由于醋酸钠的水解程度比较小,所以若溶液中四种离子的大小顺序为c(Na+)>c(OH-)>c(CH3COO-)>c(H+),这说明溶液是由醋酸钠和氢氧化钠组成的混合液,则溶液中溶质的化学式NaOH、CH3COONa。
③根据电荷守恒可知c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以若溶液中c(Na+)=c(CH3COO-),则溶液中c(OH-)=(H+),所以该溶液显中性。如果醋酸和氢氧化钠恰好中和生成醋酸钠,由于醋酸钠水解溶液显碱性。因此要使溶液显中性,则醋酸一定是过量的。因此若该溶液由体积相等的稀NaOH和CH3COOH溶液混合而成,则混合前c(NaOH)< c(CH3COOH)。
考点:考查水解平衡的应用、外界条件对水解平衡的影响以及溶液中离子浓度大小比较


科目:高中化学 来源: 题型:
2- 4 |
2- 3 |
| 滴入A溶液 |
| 再加A溶液 |
| 滴入A溶液 |
| 再加A溶液 |
| 滴入A溶液 |
| 再加A溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成




查看答案和解析>>
科目:高中化学 来源: 题型:
 (X为卤素原子)
(X为卤素原子) 的物质,该物质是一种香料.
的物质,该物质是一种香料.


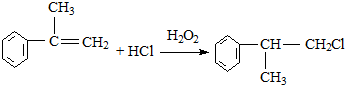
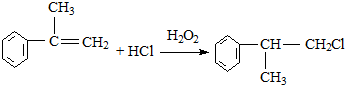


查看答案和解析>>
科目:高中化学 来源: 题型:
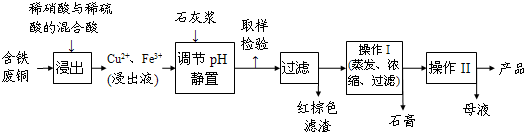
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 实验小组 | 称取CuSO4 的质量(g) |
装置C增加 的质量(g) |
量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 298.7 |
| 二 | 6.4 | 2.56 | 448 |
| ||
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com