
分析 (1)计算氢离子浓度,根据pH=-lgc(H+)来计算;
(2)2mL①与3mL②混合后氢氧化钠剩余,计算剩余氢氧化钠的浓度,计算氢离子浓度,根据pH=-lgc(H+)来计算;
(3)3mL①与2mL②混合后溶液酸剩余,计算氢离子浓度,根据pH=-lgc(H+)来计算;
(4)将①溶液稀释106后,溶液接近中性;
(5)将②溶液稀释106后,溶液接近中性.
解答 解:(1)①0.01mol•L-1的盐酸氢离子浓度为0.01mol/L,pH=-lgc(H+)=2,;②0.01mol•L-1的NaOH溶液氢氧根离子浓度为0.01mol/L,氢离子浓度为10-12mol/L,pH=-lgc(H+)=12,答:①的pH为2;②的pH为12;
(2)2mL①与3mL②混合后氢氧化钠剩余,剩余氢氧化钠的浓度=$\frac{0.01×3-0.01×2}{5}$mol/L=0.002mol/L,氢离子浓度为$\frac{1{0}^{-14}}{0.002}$mol/L=5×10-14mol/L,pH=-lgc(H+)=14-lg5=13.3,答:混合后溶液的pH为13.3;
(3)3mL①与2mL②混合后溶液酸剩余,剩余氢离子浓度$\frac{0.01×3-0.01×2}{5}$mol/L=0.002mol/L,pH=-lgc(H+)=3-lg2=2.7,答:混合后溶液的pH为2.7;
(4)将①溶液稀释106后,溶液接近中性,溶液的pH≈7,答:溶液的pH为7;
(5)将②溶液稀释106后,溶液接近中性,溶液的pH≈7,答:溶液的pH为7.
点评 本题考查学生pH的计算,注意酸碱混合后酸剩余、碱剩余溶液中氢离子浓度的计算方法是关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v1>v2 | B. | v1<v2 | C. | v1=v2 | D. | 无法肯定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 3:1:2 | C. | 6:2:3 | D. | 18:3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤①⑥③⑦ | B. | ⑤②⑥③⑦ | C. | ⑤②⑥④⑦ | D. | ⑤①⑥④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
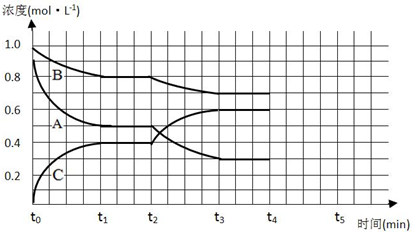
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等. ,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).
,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2 | B. | H2S | C. | S | D. | HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com