
A、CO2的电子式:
| ||||||||||||
B、Cl-的结构示意图 | ||||||||||||
| C、甲烷的结构式 CH4 | ||||||||||||
D、质量数为37的氯原子
|
 ,故A错误;
,故A错误; ,故B正确;
,故B正确; ,故C错误;
,故C错误;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第ⅠA族元素的金属性比第ⅡA族元素的金属性强 |
| B、第ⅥA族元素的氢化物中,稳定性从上到下依次减弱 |
| C、同周期非金属氧化物对应的水化物的酸性从左到右依次增强 |
| D、第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙炔的电子式:H:C:::C:H |
| B、丙烯的结构式:CH3CHCH2 |
| C、醛基的结构简式:-COH |
D、丙烷分子的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ②
②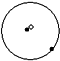 ③
③
 表示质子或电子,
表示质子或电子, 表示中子,则下列有关的叙述正确的是( )
表示中子,则下列有关的叙述正确的是( )| A、①②③为同素异形体 |
| B、①②③互为同位素 |
| C、①②③是三种化学性质不同的粒子 |
| D、①②③具有相同的质量数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(ClO)2溶液中:c(Ca2+)>c(ClO-)>c(OH-)>c(H-) |
| B、等体积、等物质的量浓度的Na2SO3溶液与NaHSO3溶液混合:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
| C、将0.2mol.L-1的某一元酸HA溶液和0.1mol.L-1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH-)+c(A-)=2c(H+)+c(HA) |
| D、某溶液中水电离出的c(OH-)=1×10-amol.L-1若a>7时,则pH该溶液的一定为14-a |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com