
【题目】A、B、C、D 四种元素,原子序数依次增大,A 原子的最外层上有4个电子;B的阴离子和 C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)C离子的结构示意图为_____。D在周期表中位置_____。
(2)A、D两元素形成的化合物属_____(填“离子”或“共价”)化合物。
(3)写出D的最高价氧化物的水化物和A单质反应的化学方程式:_____。
(4)B原子与氢原子形成的粒子中,与NH3具有相同电子数的阴离子为_____(填化学式),阳离子为_____(填化学式),其中阴离子的电子式为_____。
(5)写出B与氯元素和氢元素形成的氯水中含有的具有漂白性物质的结构式 _____________
【答案】![]() 第三周期第ⅥA族 共价 C+2H2SO4 (浓)
第三周期第ⅥA族 共价 C+2H2SO4 (浓)![]() CO2↑+2SO2↑+2H2O OH- H3O+
CO2↑+2SO2↑+2H2O OH- H3O+ ![]() H-O-Cl
H-O-Cl
【解析】
A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素。
(1)C为Na元素,钠离子的离子结构示意图为![]() ;D为S元素,在周期表中位于第三周期第VIA族,故答案为:
;D为S元素,在周期表中位于第三周期第VIA族,故答案为:![]() ;第三周期第VIA族。
;第三周期第VIA族。
(2)A为C元素、D为S元素,A、D两元素形成的化合物为CS2,属于共价化合物,故答案为:共价。
(3)D为S元素,S的最高价氧化物的水化物是硫酸,A为C元素,浓硫酸与碳单质在加热条件下反应生成二氧化碳、二氧化硫和水,其化学反应方程式为:C+2H2SO4 (浓)![]() CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4 (浓)
CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4 (浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(4)B为O元素,与氢原子能形成:H2O、H2O2、H3O+、 OH-,NH3的电子数为10,与NH3具有相同电子数的阴离子是OH-,阳离子为H3O+,OH-的电子式为:![]() ,故答案为:OH-;H3O+;
,故答案为:OH-;H3O+;![]() 。
。
(5)氯水中含有H+、Cl-、OH-、Cl2、H2O、HClO微粒,B为O元素,与氯元素和氢元素形成HClO具有漂白性,其结构式为H-O-Cl,故答案为:H-O-Cl。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.硫酸铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
C.将氯气通入氯化亚铁溶液:2Fe2++Cl2=2Fe3++2Cl-
D.将![]() 通入到
通入到![]() 溶液中:
溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、K+、NH4+、Mg2+、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种,离子浓度都为0.1mol·L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:

则关于原溶液的判断不正确的是
A.若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响
B.无法确定原溶液中是否存在Cl-
C.肯定存在的离子是SO32-、Br-,是否存在Na+、K+需要通过焰色反应来确定
D.肯定不存在的离子是Mg2+、Cu2+、SO42-、CO32-,是否含NH4+另需实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见烃,是一种水果催熟剂;草莓、香蕉中因为含有F而具有芳香味。现以A为主要原料合成F,其合成路线如下图所示。

(1)A的结构简式为____;D中官能团名称为____。
(2)写出反应①的化学方程式:____________________。
(3)写出反应②的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A(g)+ 2B(g)![]() C(g)+2D(s),经测定,在不同温度下该反应的平衡常数如下:
C(g)+2D(s),经测定,在不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 30 | 15.78 | 12.5 |
(1)该反应为__________反应(填“吸热”“放热”).平衡常数K的表达式为K=____________
(2)假设该反应在恒容绝热的密闭容器中进行,下列能判断该反应已达化学平衡状态的是________ ;
①容器中压强不变 ②混合气体中c(A)不变 ③2v正(B)=v逆(A) ④ 容器内温度不变 ⑤容器中混合气体的密度不变 ⑥ 平均摩尔质量不变 ⑦c(A):c(b):c(c)=1:2:1
A.除③以外 B.④⑤⑦ C.①②④⑤⑥ D.④⑤⑥⑦
(3)欲提高B的转化率并加快化学反应速率,下列措施可行的是_____________。(填字母)
a.在恒压下中再充入He b.向恒容体积再充入A
c.改变反应的催化剂 d.升高温度
(4)若某温度下,该反应达到平衡时测得反应物与生成物的浓度为c(A)=0.4 mol·L-1、c(B)=0.4 mol·L-1、c(C)=0.8 mol·L-1, 则此时的温度为___________;
(5)某温度下,在体积固定的1L的密闭容器中将2 mol A和2 mol B混合,测得不同时刻的压强关系如下:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 |
总压强p/MPa | 20 | 18 | 16.5 | 15 | 12.5 | 12.5 |
①计算反应到2h时v(A)=__________
②计算平衡时B的转化率为 __________,该温度下反应的平衡常数值________。
③由总压强p和起始压强p0表示反应体系的总物质的量n(总)和生成物C的物质的量n(C),则 n(总 )=________mol,n(C)=___________mol,反应物A的转化率α(A)的表达式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯与一卤代烷在催化剂作用下可生成苯的同系物:![]() +CH3X→
+CH3X→![]() +HX,在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是
+HX,在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是
A.CH2=CH2和HClB.CH3CH3和I2
C.CH2=CH2和Cl2D.CH3CH3和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,错误的是

A. 用装置①在铁上镀锌,则a为铁,b为锌
B. 装置②的总反应是:Fe+2Fe3+=3Fe2+
C. 装置③的反应实质是电解水
D. 装置④中开关由M改置于N时,Cu—Zn合金的腐蚀速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1871年门捷列夫最早预言了类硅元素锗,锗元素在元素周期表中与硅元素同族,并位于硅的下一周期。1886年德国化学家温克勒发现和分离了锗元素,并以其祖国的名字命名为“Ge”。锗是重要的的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。
已知:①丹宁是一种有机沉淀剂,可与四价锗络合形成沉淀:
②GeCl4易水解,在浓盐酸中溶解度低。
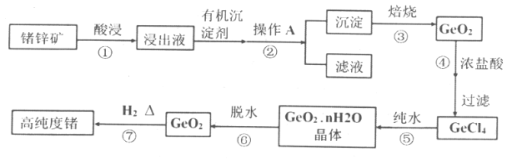
(1)锗元素的原子序数为:___________;锗元素在元素周期表中的位置是:_____________。
(2)GeCl4的结构与SiCl4相似,写出GeCl4的电子式:_______________。
(3)简述步骤①中提高酸浸效率的措施____________、_____________(写两种)。
(4)步骤②操作A是___________(填操作名称)。
(5)步骤③中的物质在___________(填仪器名称)中加热。
(6)步骤④不选用稀盐酸,而选用浓盐酸的原因可能是__________、________(写出两点)。
(7)写出步骤⑤的化学方程式________________。
写出步骤⑦的化学方程式________________。
(8)请写出一种证明步骤⑦反应完全的操作方法__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,金属—空气电池的研究和应用取得很大进步,这种新型燃料电池具有比能量高、污染小、应用场合多等多方面优点。铝—空气电池工作原理如图所示。关于金属—空气电池的说法不正确的是( )

A.铝—空气电池(如上图)中,铝作负极,电子通过外电路到正极
B.为帮助电子与空气中的氧气反应,可使用活性炭作正极材料
C.碱性溶液中,负极反应为Al(s)+3OH-(aq)=Al(OH)3(s)+3e-,每消耗2.7 g Al(s),需耗氧6.72 L(标准状况)
D.金属—空气电池的可持续应用要求是一方面在工作状态下要有足够的氧气供应,另一方面在非工作状态下能够密封防止金属自腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com