
���� ��1����KΪ����Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
����2L�ܱ������г���N2��O2��1mol��ƽ��ʱ��2min��ﵽƽ�⣬NOŨ��Ϊ0.2mol/L����֪ת���ĵ���Ϊ0.1mol/L�����v=$\frac{��c}{��t}$���㣻
��2����AgCl��s��?Ag+��aq��+Cl-��aq����֪��ƽ�������ƶ������������ʹc��Ag+��������c��Cl-��=$\frac{Ksp}{c��A{g}^{+}��}$���Դ������
��� �⣺��1���ٷ�ӦΪN2��g��+O2��g��?2NO��g������K=$\frac{{c}^{2}��NO��}{c��{N}_{2}��c��{O}_{2}��}$���ʴ�Ϊ��K=$\frac{{c}^{2}��NO��}{c��{N}_{2}��c��{O}_{2}��}$��
����2L�ܱ������г���N2��O2��1mol��ƽ��ʱ��2min��ﵽƽ�⣬NOŨ��Ϊ0.2mol/L����֪ת���ĵ���Ϊ0.1mol/L��N2����Ϊ$\frac{0.1molL}{2min}$=0.05mol/��L��min����
�ʴ�Ϊ��0.05mol/��L��min����
��2����AgCl��s��?Ag+��aq��+Cl-��aq����֪��ƽ�������ƶ������������ʹc��Ag+�������м���������ٴٽ�ƽ�������ƶ����ܢ۾������ܽ⣬����������Ũ�ȴ���������Ũ����С������ͬ�¶���c��Ag+���ɴ�С��˳���Ǣڢ٢ܢۣ�����c��Cl-��=$\frac{Ksp}{c��A{g}^{+}��}$=$\frac{1.8��1{0}^{-10}}{0.2}$=9��10-10mol/L��
�ʴ�Ϊ���ڢ٢ܢۣ�9��10-10��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����K�ı���ʽ�����ʼ��㼰���ܵ���ʵļ���Ϊ���Ĺؼ������ط�������������Ŀ��飬ע���ܽ�ƽ���ƶ���Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ý�̿��ԭSiO2��ȡ�ֹ� | |
| B�� | ������۵��Ӳ�ȴ���˿����������뵼����� | |
| C�� | ʯӢֻ�������������ά | |
| D�� | ���������ɳ���ʢ�Ÿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
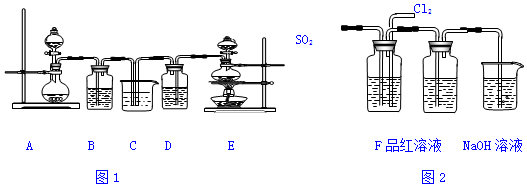
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ��ϡ���ᷴӦ��H++OH-=H2O | |
| B�� | ����ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2�� | |
| C�� | ̼������Һ��ϡ���ᷴӦ��Na2CO3+2H+=2Na++H2O+CO2�� | |
| D�� | ����������Һ��ϡ���ᷴӦ��Ba2++SO42-=BaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | RCl | B�� | RCl2 | C�� | RCl3 | D�� | RCl4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ҵ�ϴӷ�Ǧ���ص�Ǧ�����Ǧ�Ĺ����У�����̼������Һ��Ǧ�ࣨ��Ҫ�ɷ�ΪPbSO4��������Ӧ��PbSO4��s��+CO32-��aq��?PbCO3��s��+SO42-��aq����ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֣�
��ҵ�ϴӷ�Ǧ���ص�Ǧ�����Ǧ�Ĺ����У�����̼������Һ��Ǧ�ࣨ��Ҫ�ɷ�ΪPbSO4��������Ӧ��PbSO4��s��+CO32-��aq��?PbCO3��s��+SO42-��aq����ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֣�| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ�ڵ�ʵ������ͽ��� |
| ȡһ������Ʒ��ָ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ȼ��仯�������������������й㷺����;���ش��������⣺
�ȼ��仯�������������������й㷺����;���ش��������⣺| ������� | �¶�/�� | �������/L | Cl02��g����ƽ��ת���� |
| a | T1 | V1=l L | 75% |
| b | T1 | v2 | |
| c | T3 | v3 | 75% |
| d | |||
| e |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ɢϵ��ʵ������Ƿ�ɢ�����ӵ�ֱ������1-100 nm֮�� | |
| B�� | �������Һ��һ���Ǿ�һ���ķ�ɢϵ�������ö����ЧӦ������ | |
| C�� | �Ʊ�Fe��OH��3����IJ���Ϊ���ڷ�ˮ����εμ�5��6��FeCl3������Һ�������������Һ�ʺ��ɫ������ֹͣ���� | |
| D�� | �ù��˵ķ������Խ��������Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �۵�/K | �е�/K | ��״��ʱ��ˮ�е��ܽ�� | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | ������Ȼ��� |
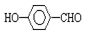 �ķе��
�ķе�� 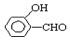 �ߣ�ԭ���ǣ�
�ߣ�ԭ���ǣ�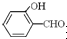 �γɷ������������
�γɷ������������ �γɷ��Ӽ���������Ӽ����ʹ���Ӽ�����������
�γɷ��Ӽ���������Ӽ����ʹ���Ӽ������������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com