
分析 W、X、Y是短周期中的三种常见元素,其原子序数依次增大,导致酸雨的主要物质是二氧化氮和二氧化硫,Y的原子序数大于W的,所以W是氮元素,Y是硫元素;X的基态原子核外有7个原子轨道填充了电子,且原子序数大于W,而小于Y,核外电子排布为1s22s22p63s23p1,所以X是铝元素,据此解答.
解答 解:W、X、Y是短周期中的三种常见元素,其原子序数依次增大,导致酸雨的主要物质是二氧化氮和二氧化硫,Y的原子序数大于W的,所以W是氮元素,Y是硫元素;X的基态原子核外有7个原子轨道填充了电子,且原子序数大于W,而小于Y,核外电子排布为1s22s22p63s23p1,所以X是铝元素.
(1)W为N元素,处于周期表中第二周期ⅤA族,N的气态氢化物是NH3,非金属性N<O,NH3稳定性比H2O弱,
故答案为:第二周期ⅤA族;二、ⅤA;弱;
(2)Y为硫元素,硫原子核外电子数为16,基态核外电子排布式为:1s22s22p63s23p4,其第一电离能比Al大,
故答案为:1s22s22p63s23p4;大;
(3)已知:①、Fe(s)+$\frac{1}{2}$O2(g)=FeO(s)△H=-272.0kJ•mol-1
②、2Al(s)+$\frac{3}{2}$O2(g)=Al2O3(s)△H=-1675.7kJ•mol-1
根据盖斯定律,②-①×3可得:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△HH=-859.7KJ/mol
故答案为:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol.
点评 本题考查结构由位置关系、核外电子排布、电离能、热化学方程式等知识点,能正确判断各元素是解本题的关键,注意书写基态原子核外电子排布式要遵循构造原理.


科目:高中化学 来源: 题型:解答题
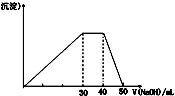 学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:
学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:| | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | SO2 |
| 第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③①②④ | C. | ④③②① | D. | ③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe跟FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | Fe跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | FeCl3与Cl2反应:Fe2++Cl2═Fe3++2Cl- | |
| D. | Fe(OH)3跟硝酸反应:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始物质的量/mol | 0.1 | 0.3 | 0 |
| 平衡物质的量/mol | 0.05 | 0.2 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+2Y?2Z | |
| C. | 若起始时X、Y、Z的物质的量分别为0.1 mol、0.4mol、0.2mol,达平衡时,Z的体积分数一定增大 | |
| D. | 若起始时X、Y、Z的物质的量分别为0.05 mol、0.15mol、0.1mol,达平衡时,X的转化率一定与原投料相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v (A)=0.5 mol/(L•s) | B. | v (B)=0.3 mol/(L•s) | C. | v (C)=0.8 mol/(L•s) | D. | v (D)=1 mol/(L•s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com