
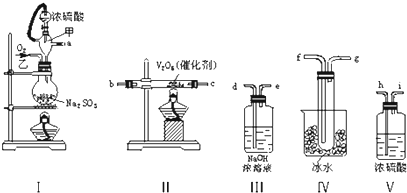
分析 (1)因从溶液中反应生成气体中混有水蒸气,所以产生的气体首先经过干燥装置Ⅲ,然后再进行二氧化硫气体的催化氧化即经过装置Ⅱ,然后是收集S03,S03的熔点是16.8℃,沸点是44.8℃,所以选择装置Ⅳ进行冷却,使三氧化硫与二氧化硫分离,最后在Ⅴ中吸收未反应的SO2,依据各装置作用排序:装置Ⅰ为气体发生装置,装置Ⅱ为二氧化硫催化氧化装置,装置Ⅲ为尾气吸收装置,装置Ⅳ为收集装置,装置Ⅴ干燥装置;
(2)甲仪器中橡皮管将分液漏斗与圆底烧瓶相连,使二者压强相等,有利于浓硫酸顺利滴入到烧瓶中;
(3)反应在加热条件下进行,为保证充分反应,应先加热;
(4)生成三氧化硫,经冷却可得到晶体;
(5)大火加热,生成二氧化硫较快,不能充分反应;
(6)二氧化硫的转化率=$\frac{二氧化硫变化量}{二氧化硫起始量}$×100%,根据硫元素守恒结合三氧化硫的量确定二氧化硫的变化量;
解答 解:(1)因从溶液中反应生成气体中混有水蒸气,所以产生的气体首先经过干燥装置Ⅲ,然后再进行二氧化硫气体的催化氧化即经过装置Ⅱ,然后是收集S03,S03的熔点是16.8℃,沸点是44.8℃,所以选择装置Ⅳ进行冷却,使三氧化硫与二氧化硫分离,最后在Ⅴ中吸收未反应的SO2,要制备二氧化硫并检验二氧化硫的性质、收集二氧化硫,依次用到的装置为:Ⅰ气体发生装置,Ⅴ干燥装置,Ⅱ为二氧化硫催化氧化装置,Ⅳ收集装置,Ⅲ尾气吸收装置,所以正确的顺序为:a h i b c f g d;
故答案为:a h i b c f g d;
(2)甲仪器中橡皮管将分液漏斗与圆底烧瓶相连,使二者压强相等,有利于浓硫酸顺利滴入到烧瓶中;
故答案为:使浓硫酸能顺利地滴入烧瓶中;维持烧瓶内压强与分液漏斗上方压强相等;
(3)为保证产生的二氧化硫尽可能多的转化为三氧化硫,应先加热V2O5,后缓缓滴入浓硫酸,
故答案为:先加热V2O5,后缓缓滴入浓硫酸;
(4)装置IV处是用来冷却三氧化硫气体,使之变成液态或固态,从而收集得到三氧化硫,所以可以在Ⅳ处看到有无色(或白色)晶体(或固体)生成,
故答案为:有无色(或白色)晶体(或固体)生成;
(5)大火加热,生成二氧化硫较快,不能充分反应,则转化率减小,故答案为:减小;
(6)n mol Na2SO3粉末与足量浓硫酸反应生成nmol二氧化硫,当反应结束时,Ⅲ处增重的部分为未反应的二氧化硫,则转化了的二氧化硫的质量为:64n-m,所以实验中SO2的转化率为$\frac{64n-m}{64n}$×100%,
故答案为:$\frac{64n-m}{64n}$×100%.
点评 本题考查物质的性质探究以及转化率的测定,把握实验的原理、物质的性质是解题关键,侧重于学生的分析能力和实验能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 凡是含碳元素的化合物都属于有机化合物 | |
| B. | 易溶于汽油、酒精、苯等有机溶剂的物质一定是有机化合物 | |
| C. | 所有的有机化合物都易燃烧 | |
| D. | 有机化合物的同分异构现象是有机化合物种类繁多的重要原因之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池工作一段时间后,KOH溶液的质量分数不变 | |
| B. | 供电时的总反应为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| C. | 氢氧燃料电池中H2和O2燃烧放出的热量转变为电能 | |
| D. | 该燃料电池可以用两个活性相同的电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤⑦ | B. | ②⑥⑦ | C. | ②④⑤⑥⑦ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
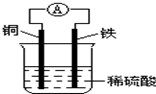
| A. | 铜棒逐渐溶解 | |
| B. | 该装置能将电能转化为化学能 | |
| C. | 负极反应式为Fe-2e-=Fe2+,发生还原反应 | |
| D. | 电子由铁棒通过导线流向铜棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A电极上发生的电极反应是还原反应 | |
| B. | A的金属性强于B | |
| C. | 电子不断由A电极经外电路流向B电极 | |
| D. | 溶液中的阳离子移向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
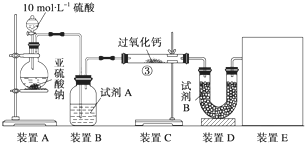
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CO(g)+3H2(g)△H=-(a+b-3C)kJ.mol-1.
CO(g)+3H2(g)△H=-(a+b-3C)kJ.mol-1.
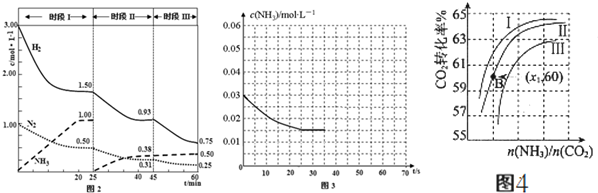
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com