
(14分)以铬铁矿(主要成分是FeO·Cr2O3,含少量MgCO3、Al2O3、SiO2等)为原料制取铬酸钠(Na2CrO4)晶体的工艺流程如下:

已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
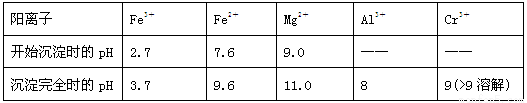
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)流程中两次使用了H2O2,分别写出反应的离子方程式:
__________________________________、____________________________________。
(2)加入NaOH调节溶液的pH=8时,被除去的离子是________;调节溶液的pH>11时,被除去的离子是________。
(3)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么?请用必要的文字和离子方程式解释:_______________________________________________________。
(4)流程图中“□”内的操作是___________________、______________________、 。
(1)2Fe2++H2O2+2H+==2Fe3++2H2O(2分)2CrO2-+3H2O2+2OH-===2CrO42-+4H2O(2分)
(2)Fe3+、Al3+ (2分) Mg2+ (2分) (3)不能(1分),当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时 Al(OH)3会溶解,引入杂质离子[Al(OH)4]- (2分)
(4)蒸发浓缩、冷却结晶、过滤 (3分)
【解析】
试题分析:(1)根据流程图可知第一次使用双氧水是为了氧化溶液中的亚铁离子以便于形成氢氧化铁沉淀而除去,反应的离子方程式为2Fe2++H2O2+2H+==2Fe3++2H2O;由于当pH>9时以CrO2-形式存在且易氧化,使用第二次加入双氧水的目的是氧化CrO2-为CrO42-,反应的离子方程式为2CrO2-+3H2O2+2OH-===2CrO42-+4H2O。
(2)根据表中数据可知pH=8时铁离子、铝已经全部转化为氢氧化物而沉淀,则被除去的离子是Fe3+、Al3+。PH大于9时镁离子就全部沉淀,则调节溶液的pH>11时,被除去的离子是Mg2+。
(3)由于当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时 Al(OH)3会溶解,从而引入杂质离子[Al(OH)4]-,使用过滤操作不能省略。
(4)从溶液中得到铬酸钠晶体的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥即可。
考点:考查物质制备工艺流程图的分析与应用


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年山西省晋中市高三1月考前适应性训练理综化学试卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数的值。下列说法错误的是
A.30g甲醛(CH2O)与30g葡萄糖均含有NA个碳原子
B.0.1molCl2与过量稀NaOH 溶液作用转移电子数0.2NA
C.常温下,1L pH=1的硫酸由水电离出的H+ 约为1×10-13NA
D.石墨电极电解CuSO4 溶液,阴极上有4mol电子转移,阳极上有NA个O2
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入FeCl2溶液中 ②过量NaOH溶液和明矾溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④向NaAlO2溶液中通入过量CO2 ⑤向饱和Na2CO3溶液中通入过量CO2
A.①③④⑤ B.①④ C.②③ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三“一诊”理综化学试卷(解析版) 题型:填空题
(16分)汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义。吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中,NaOH溶液吸收SO2也可生成Na2SO3和NaHSO3的混合溶液
①写出NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时总反应的离子方程式 。
②已知混合液pH随 :n(
:n( )变化关系如下表:
)变化关系如下表:
| 91:9 | 1:1 | 9:91 |
| 8.2 | 7.2 | 6.2 |
当混合液中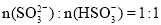 时,c(Na+) c(HSO3-)+ 2c(SO32-)(填“>”“=”或“<”)
时,c(Na+) c(HSO3-)+ 2c(SO32-)(填“>”“=”或“<”)
(2)装置Ⅱ中,酸性条件下,NO被Ce4+ 氧化的产物主要是NO3- 、NO2- ,写出只生成NO2-的离子方程式 ;
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。

①生成的Ce4+从电解槽的 (填字母序号)口流出;
②生成S2O42 - 的电极反应式为 ;
(4)已知进入装置Ⅳ的溶液中,NO2- 的浓度为a g·L- 1 ,要使1m3该溶液中的NO2- 完全转化为NO3-,至少需向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都郫县高三第二次阶诊断性考试理综化学试卷(解析版) 题型:选择题
能正确表示下列离子方程式的是
A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32—+H2O
B.铜与浓硫酸混合加热:Cu+2H2SO4(浓)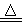 Cu2++SO42—+2H2O+SO2↑
Cu2++SO42—+2H2O+SO2↑
C.过量的浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
D.明矾溶液中滴加氢氧化钡溶液使沉淀质量最大:Al3++2SO SO42—+2Ba2++3OH- = 2BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:填空题
【化学选修-化学与技术】(15分)将磷肥生产中形成的副产物石膏(CaSO4?2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义.以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图.
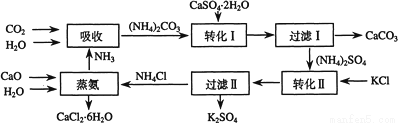
(1)本工艺中所用的原料除CaSO4?2H2O、KCl外,还需要___________________等原料.
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式_________________.
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有________(填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO32﹣的方法是__________________.
(5)已知不同温度下K2SO4在100g水中达到饱和时溶解的量如下表:
温度(℃) | 0 | 20 | 60 |
K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
60℃时K2SO4的饱和溶液591g冷却到0℃,可析出K2SO4晶体___________g.
(6)氯化钙结晶水合物(CaCl2?6H2O)是目前常用的无机储热材料,选择的依据是_______.
A.熔点较低(29℃熔化) b.能导电
c.能制冷 d.无毒
(7)上述工艺流程中体现绿色化学理念的是________________________________.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:选择题
一定条件下存在反应C(s)+H2O(g)  CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1 ℃ | T2 ℃ | T1 ℃ |
起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |

A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L-1·min-1
B.丙容器的体积V>0.5L
C.当温度为T1 ℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1< T2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:计算题
(12分)矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示。
(1)CaxMgySi8O22(OH)m改写成氧化物的形式为 ,化学式中x、y、m的代数关系式为 。
(2)对矿物样品粉末灼烧至恒重,则减少的质量与灼烧后固体中Si元素的质量比为 (用m表示)。
(3)为确定CaxMgySi8O22(OH)m的组成,进行如下实验:
①准确称取8.10g样品粉末,加入足量稀盐酸充分溶解,过滤,将沉淀灼烧得固体4.80g。
②另准确称取16.20克样品粉末在空气中灼烧,样品减少的质量随灼烧时间的变化如图所示。

根据以上实验数据计算样品的化学式(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com