
Ⅰ.2008年5月12日汶川大地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上制取漂白粉的化学方程式为______________________________________。
(2)漂白粉的有效成分是(填化学式)_______________________________。
(3)漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸。化学反应方程式为________________________________________________________________________
________________________________________________________________________。
Ⅱ.钢铁“发蓝”是在钢铁表面形成一层致密的Fe3O4薄膜的技术。其中一种方法是将钢铁制品浸到NaNO2和浓NaOH的混合溶液中加热到130℃。其过程可以用如下方程式表示:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O===3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
则反应②中的氧化剂是________(填化学式),整个过程中,每有168 g Fe参加反应,则转移________ mol 电子。
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①电解质溶液导电过程属于化学变化
②稀有气体不活泼的原因是它们原子的最外层都达到8电子稳定结构
③FeC12、CuS、NO都不能通过化合反应来制取
④SiO2是制造光导纤维的材料
A.②④ B.①④ C.①③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
向100mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是( )
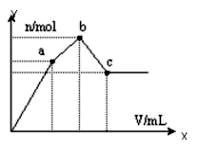 A.c点溶液呈碱性
A.c点溶液呈碱性
B.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— =
Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.a点的溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.氧化还原反应的本质是反应前后有元素化合价的升降
B.Ag++Cl-===AgCl↓的反应属于化合反应
C.从1 L 1 mol·L-1的H2SO4溶液中取出10 mL该溶液,其中H+浓度为2 mol·L-1
D.晶体硅是制造光导纤维的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.碳酸钡与盐酸反应:2H++BaCO3===Ba2++H2O+CO2↑
B.氢氧化钡溶液与稀硫酸混合:Ba2++SO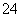 +H++OH-===BaSO4↓+H2O
+H++OH-===BaSO4↓+H2O
C.氯气通入蒸馏水:Cl2+H2O===Cl-+ClO-+2H+
D.CO2通入过量的澄清石灰水中:CO2+Ca(OH)2===CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列性质适合于某种原子晶体的是 ( )。
A.熔点1 070 ℃,易溶于水,水溶液导电
B.熔点10.32 ℃,液态不导电,水溶液导电
C.能溶于CS2,熔点112 ℃,沸点444.6 ℃
D.熔点3 550 ℃,很硬,不溶于水,不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。

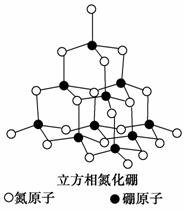
(1)基态硼原子的电子排布式为_________________________________。
(2)关于这两种晶体的说法,正确的是________(填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________________,其结构与石墨相似却不导电,原因是_________________
_________________________________________________________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为________。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 __________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有________ mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
摩托罗拉公司研发了一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应式为2CH3OH+3O2+4OH-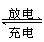 2CO
2CO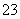 +6H2O,则下列有关说法错误的是( )
+6H2O,则下列有关说法错误的是( )
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应式为CH3OH-6e-+8OH-===CO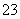 +6H2O
+6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com