
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |
 利用正、负电荷相等列方程可快速解题。
利用正、负电荷相等列方程可快速解题。 设铁的氧化物中含O2-为xmol,则其化学式为FexOy,由O2-个数守恒有:
设铁的氧化物中含O2-为xmol,则其化学式为FexOy,由O2-个数守恒有: 2yH++ FexOy = yH2O+ xFe+(2y/x)
2yH++ FexOy = yH2O+ xFe+(2y/x) 2ymol ymol
2ymol ymol 0.7mol amol
0.7mol amol 2y:y=0.7:a a=0.35(mol)
2y:y=0.7:a a=0.35(mol) 设FexOy中含Fe2+bmol,则:
设FexOy中含Fe2+bmol,则: 2Fe2++ Cl2 = Fe3++ 2Cl-
2Fe2++ Cl2 = Fe3++ 2Cl-  2mol 22.4L
2mol 22.4L bmol 0.56L
bmol 0.56L 2:b=22.4:0.56 b=0.05(mol)
2:b=22.4:0.56 b=0.05(mol) 设样品FexOy中含Fe3+为cmol,则由电荷守恒可得:
设样品FexOy中含Fe3+为cmol,则由电荷守恒可得: (2×0.05mol)×3cmol=2×0.35mol
(2×0.05mol)×3cmol=2×0.35mol 解之得c=0.2mol
解之得c=0.2mol 故样品FexOy中:x:y=(0.05+0.02):0.35=5:7
故样品FexOy中:x:y=(0.05+0.02):0.35=5:7 即样品“氧化铁”化学式为:Fe5O7。
即样品“氧化铁”化学式为:Fe5O7。

科目:高中化学 来源:不详 题型:填空题
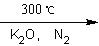 (C5H5)2 Fe+H2。
(C5H5)2 Fe+H2。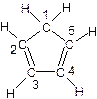 (图中数字仅代表碳原子编号),在其5个碳原子中采取sp3杂化的是 (填写编号),
(图中数字仅代表碳原子编号),在其5个碳原子中采取sp3杂化的是 (填写编号),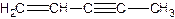 是环茂二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有 个;
是环茂二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有 个;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 (1)铜与浓硝酸反应的化学方程式:_______________________;
(1)铜与浓硝酸反应的化学方程式:_______________________; (2)实验中观察到的主要现象是:
(2)实验中观察到的主要现象是: ①_______________________________ ;
①_______________________________ ; ②_______________________________ ;
②_______________________________ ; ③_______________________________ ;
③_______________________________ ; ④_______________________________ 。
④_______________________________ 。 (3)用该装置做铜与浓硝酸反应实验的优点:______________ ;
(3)用该装置做铜与浓硝酸反应实验的优点:______________ ; (4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。
(4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.1.5mol/L | B.0.5mol/L | C.2mol/L | D.1.2mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.MgCO3、MgO、Mg3N2 | B.Mg(OH)2、MgO、MgCO3 |
| C.MgO、Mg3N2、C | D.Mg2N3、C、MgO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com