
溶液的pH、体积相同的盐酸和醋酸两种溶液,下列叙述错误的是
A.它们与NaOH完全中和时,醋酸溶液所消耗的NaOH少
B.它们分别与足量CaCO3反应时,放出的CO2一样多
C.两种溶液的n(Cl-)= n(CH3COO-)相同
D.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-)
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:2015-2016学年湖北省高二5月月考化学试卷(解析版) 题型:选择题
下列有关有机物研究方法的说法中,不正确的是( )
A.应用李比希法、钠熔法、铜丝燃烧法、元素分析仪都可确定有机化合物的元素组成。
B.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物组成元素和结构的分析
C.运用同位素示踪法可确定有机物的反应机理
D.可用酸性高锰酸钾溶液或溴水鉴定某有机物分子中是否含有碳碳双键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:选择题
Diels-Alder反应为共轭双烯与含有烯键或炔键的化合物相互作用生成六元环状化合物的反应,最简单的反应是 。如果要合成
。如果要合成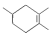 ,所用的原始原料可以是( )
,所用的原始原料可以是( )
A.2-甲基-1,3-丁二烯和2-丁炔
B.2,3-二甲基-l,3-丁二烯和丙烯
C.2,3-二甲基-1,3-戊二烯和乙烯
D.1,3-戊二烯和2-丁烯
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨六中高三下三模理综化学试卷(解析版) 题型:选择题
分子式为C6H12的烯烃含有3个甲基的同分异构体有(不考虑立体异构)
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:实验题
某研究小组利用乳酸钙和FeCl2为原料生产乳酸亚铁([CH3CH(OH) COO]2Fe·3H2O) 和医用二水合氯化钙晶体(CaCl2·2H2O的质量分数为97.3% ~99.3%),制备流程如下:
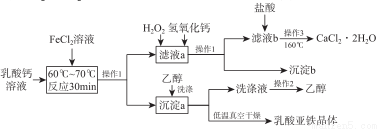
(1)实验室常用两种方案制备FeCl2,写出原子利用率为100%的反应的化学方程式 ;在FeCl2溶液中需要加
(2)制备乳酸亚铁晶体是向乳酸钙溶液中加入过量的FeCl2溶液,写出该反应的化学方程式 。
(3)操作1、操作2、操作3依次为 、 、 。
(4)向“滤液a”中先加H2O2溶,作用是 。然后再调节溶液
的 pH 约为5,目的是 。
(5)向“滤液b”加盐酸的目的是 。
(6)为测定样品中CaCl2·2H2O的含量,称取0.7600g样品并配成250mL 溶液,各取该溶液 25.00mL,分别置于三个锥形瓶中,用0.05000mol·L -1 AgNO3溶液进行三次滴定,消耗AgNO3溶液的平均体积为20.39mL。计算样品中CaCl2·2H2O的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.碳酸氢钠溶液与少量石灰水反应:HCO3-+OH-+Ca2+===H2O+CaCO3↓
B.氯化铵与氢氧化钠溶液混合:NH4++OH-===H2O+NH3↑
C.向漂白粉溶于水形成的溶液中通入少量的SO2:Ca2++3ClO-+SO2+H2O===CaSO4↓+Cl-+2HClO
D.硫化亚铁溶于稀硝酸中:FeS+2H+===Fe2++H2S↑
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
已知:2R—Cl+2Na→R—R+2NaCl(R代表烃基),下列有机物通过上述反应可制得对二甲基环己烷的是
A.2,3—二氯丁烷
B.1,3—二氯丁烷
C.2—氯丁烷
D.2,5—二氯己烷和1,2—二氯乙烷
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.向NaAlO2溶液中通入过量CO2:CO2+AlO2-+2H2O=Al(OH)3?+HCO3-
B.NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH- NH3?+H2O
NH3?+H2O
C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2?
D.Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO?+H2O
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三5月高考模拟理综化学试卷(解析版) 题型:实验题
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:

(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为____________,该操作将I2还原为I-的目的是____________;
(2)操作X的名称为____________;
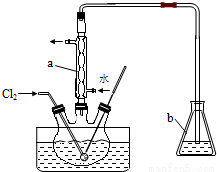
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示).实验室控制在较低温度下进行的原因是____________;仪器b中盛放的溶液为_____。
(4)已知:5SO32-+2IO3-+2H+═I2+5SO42-+H2O
某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种,请补充完整检验含碘废水中是否含有I-、IO3-的实验方案:(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
①取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在:
②____________;
③另从水层取少量溶液,加入1-2mL淀粉试液,加盐酸酸化,滴加Na2SO3溶液,若溶液变蓝色,说明废水中含有IO3-,否则说明废水中不含IO3-。
(5)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用ClO2氧化酸性含I-废液回收碘。
①完成ClO2氧化I-的离子方程式:□ClO2+□I-+□____________=□I2+□Cl-+□____________
②若处理含I-相同量的废液回收碘,所需Cl2的物质的量是ClO2的____________倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com