
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 原子个数比 | B:A=1:3 | C:A=1:2 | D:A=1:1 | E:A=1:1 |
| A. | 元素E在元素周期表中的位置为第三周期、VIIA族 | |
| B. | 原子半径:A<B<C<D | |
| C. | 甲和丙分子均只含极性键 | |
| D. | A、B、C、D四种元素中的三种能形成多种与甲分子等电子数的化合物 |
分析 A、B、C、D、E五种短周期元素,其原子序数逐渐增大,元素A的单质是密度最小的气体,则A为H元素;元素B的单质存在两种以上同位素异形体,且其中一种是自然界中硬度最大的单质,则B为碳元素;元素D的最外层电子数是次外层电子数的三倍,原子只能有2个电子层,最外层电子数为6,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B、C、D、E四种元素均能与A形成等电子数的四种分子,结合化合物中各原子的个数比,可知甲为C2H6,乙为N2H4,丙为H2O2,可推知E为Cl,丁为HCl,据此解答.
解答 解:、B、C、D、E五种短周期元素,其原子序数逐渐增大,元素A的单质是密度最小的气体,则A为H元素;元素B的单质存在两种以上同位素异形体,且其中一种是自然界中硬度最大的单质,则B为碳元素;元素D的最外层电子数是次外层电子数的三倍,原子只能有2个电子层,最外层电子数为6,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B、C、D、E四种元素均能与A形成等电子数的四种分子,结合化合物中各原子的个数比,可知甲为C2H6,乙为N2H4,丙为H2O2,可推知E为Cl,丁为HCl.
A.元素E为Cl,在元素周期表中的位置为第三周期VIIA族,故A正确;
B.同周期自左而右原子半径减小,所有元素中H原子半径最小,故原子半径H<O<N<C,故B错误;
C.甲为C2H6,丙为H2O2,C2H6电子中碳原子之间、H2O2分子中氧原子之间均形成非极性键,故C错误;
D.H、C、N、O四种元素中的三种能形成CH3OH、NH2OH、CH3NH2等,与甲分子等电子数,故D正确,
故选AD.
点评 本题考查元素化合物推断,推断元素是解题关键,D选项中注意利用替换法书写18电子微粒,难度中等.


科目:高中化学 来源: 题型:多选题
| A. | Na2O2中既含离子键又含非极性键 | |
| B. | BF3分子中的所有原子共平面 | |
| C. | SiO2和Na2O2的晶体类型相同 | |
| D. | S的第一电离能大于P的第一电离能. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原子序数依次增大的前四周期五种元素X、Y、Z、M、W.已知X的一种单质是原子晶体,且是自然界中最坚硬的物质,Y原子最外层电子数是次外层的3倍,M与Y同主族,且M元素的单质为淡黄色;Z与M同周期,且Z元素与Y元素可以形成两种化合物,其中一种化合物也为淡黄色;W是生活中使用最广泛的金属元素,且有+2和+3两种常见化合价.据此回答:
原子序数依次增大的前四周期五种元素X、Y、Z、M、W.已知X的一种单质是原子晶体,且是自然界中最坚硬的物质,Y原子最外层电子数是次外层的3倍,M与Y同主族,且M元素的单质为淡黄色;Z与M同周期,且Z元素与Y元素可以形成两种化合物,其中一种化合物也为淡黄色;W是生活中使用最广泛的金属元素,且有+2和+3两种常见化合价.据此回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
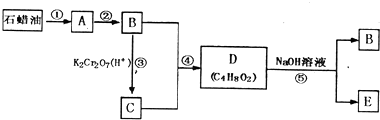
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇所含的分子数为NA | |
| B. | 1mol/LCaCl2溶液中含有的氯离子数目为2NA | |
| C. | 1 mol金属钠在足量氧气中完全燃烧转移的电子数为2NA | |
| D. | 28g N2中含有的原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 石墨烯是由碳原子构成的单层片状结构的新材料(如图),可由石墨剥离而成,具有极好的应用前景.下列说法正确的是( )
石墨烯是由碳原子构成的单层片状结构的新材料(如图),可由石墨剥离而成,具有极好的应用前景.下列说法正确的是( )| A. | 石墨烯与金刚石互为同位素 | |
| B. | 0.12g石墨烯中含有6.02×1021个碳原子 | |
| C. | 石墨烯中的碳原子间以共价键结合 | |
| D. | 石墨烯是一种新型有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 稀硫酸滴入碳酸钠溶液中,将产生的气体通入盛有硅酸钠溶液的烧杯中 | 烧杯中产生白色胶状沉淀 | 非金属性:S>C>Si |
| B | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 该溶液一定是钠盐溶液 |
| C | 将饱和氯化铁溶液滴入盛有沸水的烧杯中,继续煮沸至溶液呈红褐色,停止加热,用激光笔照射烧杯中的液体 | 看到一条光亮的“通路” | 证明生成了氢氧化铁沉淀 |
| D | 在分液漏斗中加入碘水后再加入CCl4,充分振荡、静置 | 分层,且上层溶液呈紫色 | CCl4可作为碘的萃取剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 59 | B. | 102 | C. | 114 | D. | 150 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||||
| Y | Z | |||
| W |
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) | |
| B. | Y、Z的氢化物有可能含非极性键 | |
| C. | Z、W形成的化合物W显负价 | |
| D. | Y分别与Z、W形成的化合物全部都是非极性分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com