
| 1000ρw% |
| M |
| 1000ρw% |
| M |
1000×1.08×
| ||
| 174 |
| 11.1 |
| 100+11.1+150 |


科目:高中化学 来源: 题型:
| A、如果苯酚浓溶液沾到皮肤上,应立即用稀氢氧化钠溶液清洗 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
| C、不慎将酒精洒到桌面上引起着火,应立即用较多的水浇灭 |
| D、蒸发溶液时有液滴飞溅,应立即加水冷却 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ?mol-1 | ||
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3 kJ?mol-1 | ||
| C、2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ?mol-1 | ||
D、CO(g)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
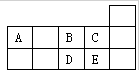 如表为元素周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )
如表为元素周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )| A、A与B形成的阴离子可能有:AB32-、A2B42- |
| B、E的氢化物的沸点比C的氢化物的沸点低 |
| C、D在过量的B中燃烧的主要产物为DB3 |
| D、这5种元素形成只含极性键的非极性分子多于4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4Q1+0.5Q3 |
| B、4Q1+0.5Q2 |
| C、4Q1+Q3 |
| D、4Q1+2Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的HX与pH=11的YOH等体积混合,所得溶液的pH一定为7 |
| B、在0.1 mol/L(NH4)2Fe(SO4)2溶液中c(H+)+c(NH4+)+c(Fe2+)=c(OH-)+c(SO42-) |
| C、向醋酸钠溶液中加入适量醋酸,所得酸性溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、0.4 mol/LHCl与0.1 mol/L NaAlO2等体积混合,所得溶液中c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
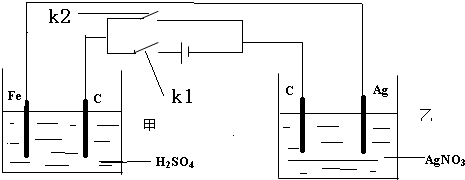
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com