
【题目】胶体、浊液与溶液溶液的本质区别在于( )
A.分散系是否有丁达尔现象
B.分散质粒子是否带电荷
C.分散系是否稳定
D.分散质粒子直径的大小
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答相关的问题。
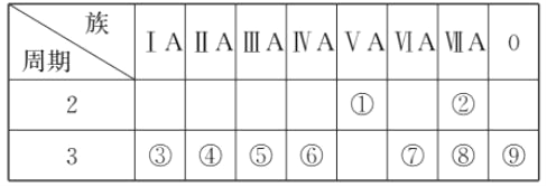
(1)写出④的元素符号________。
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:___________________________。
(3)在这些元素中,最高价氧化物的水化物酸性最强的是________(填相应化学式,下同),碱性最强的是________。
(4)这些元素中(除⑨外),原子半径最小的是________(填元素符号,下同),原子半径最大的是________。
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2 , (O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为(方程式中用具体元素符号表示) _____________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某铅蓄电池的正、负极标记被磨损,试用如图装置设计实验,识别出此铅蓄电池的正、负极。
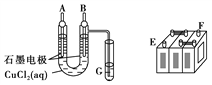
①若A接E,B接F,而B电极出现____________现象,电极反应式为_______________,则说明F为正极。
②铅蓄电池工作时(放电),其E所在电极的电极反应式为 ________,充电时该极与外接电源的________极相连。
③若有0.2 mol电子发生转移,则正极消耗的PbO2的物质的量是________。
(2)利用甲醇(CH3OH)、氧气组成燃料电池,电解质溶液为碱性,电池工作时,其负极反应式为________________________________________________________________________
(3)一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+,正极的反应式:_____________________________;电池反应的总方程式为____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是当前应用最广泛的金属材料之一,铝制品及其化合物在日常生活和工农业生产中也有着重要的用途。回答下列问题:
(1)基态铝原子的核外电子排布式为____________。
(2)根据元素周期律等知识判断,第一电离能Al____________Mg(填写“大于”或“小于”)。
(3)Al2O3是常用的耐火材料,工业上也是用电解Al2O3方法制取金属Al,据此判断Al2O3的晶体类型是____________。
(4)LiAlH4是一种重要的有机合成试剂,AlH4-的立体构型为____________,LiAlH4中Al原子的杂化轨道类型为____________。
(5)金属铝的晶胞结构如图1所示,原子之间相对位置关系的平面图如图2所示。

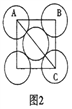
①晶体铝中原子的堆积方式为____________。
②已知铝原子半径为acm,摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则晶体铝的密度ρ=_______g·cm-3(用含a、M、NA的代数式来表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CH2=C(CH3)2和![]() 为原料可制备香料E(C11H12O2),其合成路线如下:
为原料可制备香料E(C11H12O2),其合成路线如下:
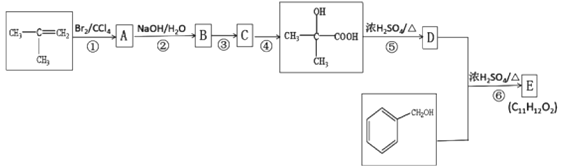
已知C 能发生银镜反应,D能使酸性高锰酸钾溶液褪色。请回答下列问题:
(1) 根据系统命名法有机物CH2=C(CH3)2的名称为___________;
(2) C 中能发生银镜反应的官能团名称是___________;
(3) ⑤的反应类型是_________;
(4) 写出⑥反应的化学方程式:__________________;
(5) 含苯环的![]() 的同分异构体有______种(不包含
的同分异构体有______种(不包含![]() ),其中核磁共振氢谱图有4 組峰且能与FeCl3溶液发生显色反应的有机物的结构简式为________;
),其中核磁共振氢谱图有4 組峰且能与FeCl3溶液发生显色反应的有机物的结构简式为________;
(6) 参照上述合成路线设计一条由乙烯制备聚乙二酸乙二酯的合成路线(无需注明反应条件)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,X与M同主族,Z的气态氢化物能与其最高价氧化物的水化物反应,G是地壳中含量最高的金属元素。清回答下列问题:
(1)Q的元素符号为______,Y、Z、M、G四种元素原子半径由大到小的顺序是(写元素符号)_______。
(2)Y在元素周期表中的位置为_______________,Y与硫元素形成的二元化合物的电子式为_________________________。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)_____________。
(4)单质Y和元素Z的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为_________。
(5)Z和G组成的化合物GZ,被大量用于制造电子元件。工业上用G的氧化物、Y单质和Z单质在高温下制备GZ,其中G的氧化物和Y单质的物质的量之比为1∶3,则该反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各物质按酸、碱、盐分类顺序排列,正确的是 ( )
A.盐酸、烧碱、胆矾B.硫酸、纯碱、食盐
C.碳酸、乙醇、醋酸钠D.磷酸、熟石灰、苛性钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com