
【题目】Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用。
(1)N位于周期表中第 周期 族,与N3-含有相同电子数的三原子分子的空间构型是 。
(2)C、N、O三种元素的第一电离能由大到小的顺序为
(3)Cu+电子排布式为 ,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu,但CuO在高温下会分解成Cu20,试从结构角度解释高温下CuO何会生成Cu2O: 。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙醛,乙醛分子中碳原子的杂化方式是 ,乙醛分子中H—C—O的键角 (填“大于”“等于”或“小于”)乙醇分子中的H—C一0的键角。
(5)[Cu(H20)4]2+为平面正方形结构,其中的两个H20被Cl-取代有两种不同的结构,试画出[Cu(H20)2(C1)2]具有极性的分子的结构式: 。
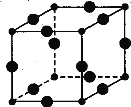
(6)Cu3N的晶胞结构如图,N3-的配位数为 ,Cu+半径为a pm,N3- 半径为b pm,Cu3N的密度为 g·cm-3。(阿伏加德罗常数用NA表示)
【答案】(1)二 VA V形 (2)N>O>C (3)1s22s22p6 3s23p63d10
Cu+价电子排布式为3d10,为全充满结构,更稳定
(4)sp2、sp3 大于 (5) (6)6
(6)6 ![]()
【解析】
试题分析:(1)N元素位于元素周期表中第二周期第VA族;N3-中的电子数是10个,所以与N3-含有相同电子数的三原子分子是水分子,水分子的空间构型是V型;
(2)同周期元素随核电荷数的增大,第一电离能逐渐增大,但N原子的2p轨道为半充满的稳定状态,所以N的第一电离能大于O,所以C、N、O的第一电离能的大小顺序是N>O>C;
(3)Cu+的核外有28个电子,最外层的4s1电子失去,所以电子排布式为1s22s22p6 3s23p63d10;CuO中Cu为+2价,而+1价Cu价电子排布式为3d10,为全充满结构,更稳定;
(4)乙醛的结构简式我CH3CHO,甲基的C原子周围的化学键都是单键,是sp3杂化,而醛基中的C原子存在双键,所以是sp2杂化;乙醇分子中与醛基相连的C原子也是sp3杂化,受孤对电子的影响,所以sp2杂化的键角大于sp3杂化的键角;
(5)[Cu(H20)4]2+为平面正方形结构,其中的两个H20被Cl-取代且具有极性的分子不是中心对称分子,所以该分子的结构为 ;
;
(6)根据原子半径的大小,打球代表Cu原子,小球代表N,N3-的配位数为6,同层为4个,上下各一个;该晶胞中Cu原子的个数是12×1/4=3,N原子的个数是8×1/8=1,晶胞的体积是[(2a+2b)×10-10cm]3,晶胞质量是(3×64+14)/NA,所以晶胞的密度=m/V=206/8(a+b)3×10-30×NA g·cm-3=103×1030/4(a+b)3 NA g·cm-3。


科目:高中化学 来源: 题型:
【题目】下列有关化学反应与能量变化的说法正确的是

A.甲烷的燃烧热△H=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+![]() O2(g)=CO(g)+2H2O(g) ΔH=-890.3kJ·mol-1
O2(g)=CO(g)+2H2O(g) ΔH=-890.3kJ·mol-1
B.相同条件下,氢气和氧气反应生成液态水比生成等量的气态水所放出的热量少
C.根据右图金刚石在一定条件下转化成石墨提供的信息,可知生成物比反应物稳定,向外界放出的热量为E2 -E3
D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍有广泛的用途,粗镍中含有少量Fe、Zn、Cu、Pt等杂质,以硫酸镍 溶液为电解液进行粗镍 提纯,下列说法正确的是(已知:氧化性的强弱顺序为Fe2+<Ni2+<Cu2+)
A. 阳极首先发生的电极反应是Ni2++2e-=Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在金属阳离子只有Fe2+和Zn2+
D. 电解后,Cu和Pt沉积在电解槽底部形成阳极泥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列叙述错误的是
A.SO2可用于漂白纸浆B.SiO2可用于制光导纤维
C.NaClO溶液可用于杀菌消毒D.Cu(OH) 2可用作口服制酸剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O是_____色固体,与水反应的化学方程式为___________。Na2O2是_____色固体,与水反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为M gmol﹣1 . 若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为mol.
(2)该气体所含原子总数为个.
(3)该气体在标准状况下的体积为L.
(4)该气体在标准状况下的密度为g/L.
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)有以下10种物质:①铁 ②稀硫酸 ③氯化氢 ④氨气 ⑤空气 ⑥二氧化碳 ⑦水银 ⑧氯化镁 ⑨硫酸钡=10 ⑩蔗糖.其中属于电解质的是 .
(2)写出⑧在水溶液中的电离方程式 .
(3)写出①与水蒸气反应的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com