
【题目】W、X、Y、Z、M、N六种主族元素,它们在周期表中位置如图所示,下列说法正确的是( )
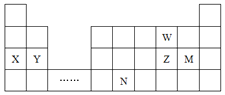
A.原子半径:![]() 简单离子半径:
简单离子半径:![]()
B.单质的还原性:![]() 简单氢化物的沸点:
简单氢化物的沸点:![]()
C.溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D.元素N位于金属与非金属的分界线附近,可以推断N的单质可作半导体材料
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,1 L 己烷完全燃烧后,所生成的气态产物的分子数为![]() NA
NA
B.10 g 46%的乙醇溶液中氢原子的个数为 0.6 NA
C.28 g 乙烯与丙烯的混合气体,共用的电子对数为 6 NA
D.100 mL 0.1 mol/L CH3COOH 溶液跟足量乙醇、浓硫酸共热,发生酯化反应,生成乙酸乙酯分子 数为 0.01 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不能达到相应实验目的的是
选项 | 实验操作 | 实验目的 |
A | 向苯与液溴的混合液中加入铁粉,将产生的气体直接通入AgNO3溶液中 | 验证液溴与苯发生取代反应 |
B | 向5mL浓度为0.5mol·L-1的KI溶液中滴加少量氯化铁溶液,再加入少量淀粉溶液,振荡 | 比较I-、Fe2+的还原性强弱 |
C | 向5mL浓度为0.2mol·L-1的MgCl2溶液中滴加少量NaOH溶液,待有白色沉淀生成后,再滴加0.2mol·L-1的CuCl2溶液 | 比较Cu(OH)2、Mg(OH)2溶度积的大小 |
D | 向 | 验证与H+的结合能力: |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A.第ⅠA族的金属元素是同一周期中金属性最强的元素
B.P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强
C.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
D.主族元素原子的最外层电子数不一定等于该元素的最高正化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )
A | B | C | ||
D | ||||
A.原子半径大小比较为D>C>B>A
B.生成的氢化物分子间均可形成氢键
C.A与C形成的阴离子可能有AC![]() 、A2C
、A2C![]()
D.A、B、C、D的单质常温下均不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物![]() (
(![]() )、
)、![]() (
(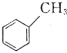 )、
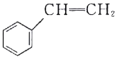
)、![]() (
( )的说法正确的是( )。
)的说法正确的是( )。
A.![]() 和
和![]() 的一氯代物均有三种结构
的一氯代物均有三种结构
B.![]() 和
和![]() 互为同分异构体,
互为同分异构体,![]() 和
和![]() 互为同系物
互为同系物
C.![]() 、
、![]() 、
、![]() 分子中的所有原子可能在同一平面上
分子中的所有原子可能在同一平面上
D.![]() 、
、![]() 、
、![]() 三种物质均能使酸性KMnO4溶液褪色
三种物质均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的![]() (如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关
(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关![]() 的说法正确的是
的说法正确的是
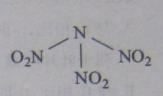
A. 分子中N、O间形成的共价键是非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 15.2g该物资含有6.02×![]() 个原子
个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列结论中正确的是( )
A.25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
B.粗铜精炼时,当阳极质量减少6.4g时,电路中转移电子数一定不是0.2NA
C.含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
D.200mL0.5mol/LNa2CO3溶液中,由于CO32-水解,所以阴离子数目小于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列粒子![]() 分子或离子
分子或离子![]() 均含有18个电子:
均含有18个电子:
粒子 | A+ | B2- | C | D | E | F |
组成特点 | 单核离 | 化合物, 双核分子 | 单质, 双核分子 | 化合物, 三核分子 | 化合物, 四核分子 | |
下列说法错误的是
A.A的元素符号是K,B2-的离子结构示意图是![]()
B.C的浓溶液可用于实验室制Cl2
C.D的单质具有强氧化性,可将其同族元素的单质从盐溶液中置换出来
D.F中可能既含极性键又含非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com