
(12分) X、Y、Z三种短周期元素,两两之间能组成5种化合物A、B、C、D、E;X、Y、Z三种元素可组成化合物F。已知:化合物A、B、C中原子个数比都为1︰1;B为淡黄色固体,C、E常温下均为无色液体;A是化学式为XZ的离子化合物,A与E反应生成F和一种气体;D是化学式为X2Y的离子化合物,D的阴、阳离子具有相同的电子层结构且与E分子所含电子数相等。 请回答下列问题:
(1)X元素的名称是________________。
(2)X、Y、Z的原子半径从大到小的顺序是(用元素符号表示)____________________。
(3)写出F的电子式______________________________。
(4)已知X单质、A、B、D固体,分别与E反应都生成同一种物质,其中X单质、A、B分别与E的反应均是氧化还原反应。请写出X单质、B分别与E反应的化学方程式___________, ;
B中含有的化学键是 ;请举一例说明B的用途_____________。
(5)请写出由化合物C制取Y的单质反应的化学方程式_______________________________。
(1)钠 (2) Na>O>H (3)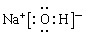
(4)2Na+2H2O=4NaOH+H2↑;2Na2O2+2H2O=4NaOH+O2↑;离子键和非极性键;作呼吸面具和潜水艇里氧气得来源 (5)2H2O2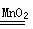 2H2O+O2
2H2O+O2
解析试题分析:(1)B为淡黄色固体可推测为Na2O2,三种元素中有Na和O。C、E常温为液体,推测为H2O2和H2O,可知三种元素还包括H。A为XZ的离子化合物,可知A为NaH,X为Na,Y为O,Z为H.则A为NaH,B为Na2O2,C为H2O2,D为Na2O,E为H2O,F为NaOH.故X元素的名称是:钠。(2)同周期从左到右半径逐渐减小,同主族从上到下逐渐增大,X、Y、Z的原子半径从大到小的顺序是(用元素符号表示):Na>O>H。
(3)F的化学式:NaOH,F的电子式: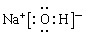 。
。
(4)X为Na,B为Na2O2,E为H2O,X单质、B分别与E反应的化学方程式:2Na+2H2O=4NaOH+H2↑、2Na2O2+2H2O=4NaOH+O2↑,B是过氧化钠,含有钠离子和过氧根离子.故含离子键,过氧根离子内两个氧原子间是非极性键。
(5)C为H2O2,Y为O,反应的化学方程式:2H2O2 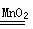 2H2O+O2↑。
2H2O+O2↑。
考点:考查元素周期表,原子结构,元素及其化合物的性质,化学键


科目:高中化学 来源: 题型:单选题
质量数为A,核内中子数为N的R2+离子与16O所形成的Wg氧化物中所含质子的物质的量为 ( )
A. mol mol | B.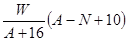 mol mol |
| C.(A-N+8)mol | D.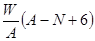 mol mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中,正确的是
| A.同周期元素中,ⅦA族元素的原子半径最大 |
| B.ⅥA族元素的原子,其半径越大,越容易得到电子 |
| C.室温时,0族元素的单质都是气体 |
| D.元素周期表中,从ⅢB到ⅡB这10个纵行的元素都是副族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、质量数为293的超重元素,该元素原子核内的中子数与核外电子数之差为
| A.47 | B.57 |
| C.61 | D.175 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D四种原子序数依次增大的元素,分布在三个不同的短周期,其中B与C为同一周期的相邻元素,A与D为同一主族。C的单质是燃料电池的一种原料,D是所在周期原子半径最大的元素。下列说法正确的是( )
A.原子半径:D>C>B>A
B.B的氢化物沸点比C的氢化物的沸点高
C.A与D可形成化合物DA,1mol该物质可与水反应转移的电子数为NA
D.由A、B、C形成的化合物一定只有共价键没有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
元素周期表是学习物质结构和性质的重要工具。请参照元素①-⑦在周期表中的位置,回答下列问题:
| ① | | | ||||||
| | | | | ② | ③ | ④ | | |
| ⑤ | | ⑥ | ⑦ | | | | | |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA的单质能跟足量的盐酸反应,在标准状况下可置换出22.4L的H2,这时A转变为与氖原子具有相同电子层结构的离子。试回答:
(1)写出A和C组成的化合物的电子式________________________________;
(2)B的离子结构示意图是 ,与B的离子具有相同电子数的分子中,有一种分子可与盐酸化合生成一种盐,该盐的化学式是 ;
(3)写出C元素的单质和甲烷发生一元取代反应的化学方程式____________________ ;
(4)写出A最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ① | ② | | | |
| 3 | ③ | ④ | ⑤ | ⑥ | | ⑦ | ⑧ | ⑩ |
| 4 | | | | | | | ⑨ | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(7分)五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物的水溶液呈碱性,C和E形成的化合物的水溶液呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 (填元素符号);
(2)B、D所形成的最简单的氢化物中沸点较高的是 (填化学式),原因是 。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为 ,其中存在的化学键类 型为 ;
(4)D与E形成的化合物中,所有原子均能满足8电子稳定结构的物质的电子式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com