
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ķł0.10 mol”¤L£1µÄ°±Ė®ÖŠ¼ÓĖ®ŗó£¬NH3”¤H2OµÄµēĄė³Ģ¶ČŗĶc(OH£)¾łŌö“ó
B£®ŅņĪŖ“×ĖįŹĒČõµē½āÖŹ£¬ŃĪĖįŹĒĒæµē½āÖŹ£¬Ņņ¶ųÖŠŗĶµČĢå»żµČĪļÖŹµÄĮæÅØ¶ČµÄ“×ĖįŗĶŃĪĖįŹ±£¬ÖŠŗĶŃĪĖįĻūŗĵÄĒāŃõ»ÆÄʱČÖŠŗĶ“×Ėį¶ą
C£®25”ꏱ£¬ČĪŗĪŅŌĖ®ĪŖČܼĮµÄĻ”ČÜŅŗÖŠc(H£«)”¤c(OH£)£½1”Į10£14
D£®pHĻąĶ¬µÄ¢ŁCH3COONa¢ŚNaHCO3¢ŪNaClOČżÖÖČÜŅŗµÄc(Na£«)£ŗ¢Ū£¾¢Ś£¾¢Ł
 ½šŌæ³×ŹŌ¾ķĻµĮŠ“š°ø
½šŌæ³×ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗžÄĻ³£µĀŹÆĆŵŚŅ»ÖŠŃ§ø߶žÉĻĘŚÖŠĄķ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŹŅĪĀĻĀĻņ10mL pH£½3µÄ“×ĖįČÜŅŗÖŠ¼ÓČė10mLĖ®Ļ”ŹĶŗó£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ČÜŅŗÖŠµ¼µēĮ£×ӵďżÄæ¼õÉŁ
B£®ČÜŅŗÖŠ ²»±ä
²»±ä
C£®“×ĖįµÄµēĄė³Ģ¶ČŌö“ó£¬c£ØH+£©ŅąŌö“ó
D£®ŌŁ¼ÓČė10mlpH£½11µÄNaOHČÜŅŗ£¬»ģŗĻČÜŅŗpH£½7
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”¼ĪŠĖ”¢ŗ¼ÖŻ”¢Äž²ØĪ劣øßČżÉĻµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ČĖĄą»ī¶Æ²śÉśµÄCO2³¤ĘŚ»żĄŪ£¬ĶžŠ²µ½ÉśĢ¬»·¾³£¬Ęä¼õÅÅĪŹĢāŹÜµ½Č«ŹĄ½ē¹Ų×¢”£
£Ø1£©¹¤ŅµÉĻ³£ÓĆøßÅØ¶ČµÄK2CO3 ČÜŅŗĪüŹÕCO2£¬µĆČÜŅŗX£¬ŌŁĄūÓƵē½ā·ØŹ¹K2CO3 ČÜŅŗŌŁÉś£¬Ęä×°ÖĆŹ¾ŅāĶ¼ČēĻĀ£ŗ
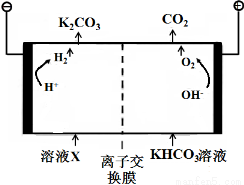
ŌŚŃō¼«Ēų·¢ÉśµÄ·“Ó¦°üĄØ ŗĶH ++ HCO3- === H2O + CO2”ü”£
¼ņŹöCO32-ŌŚŅõ¼«ĒųŌŁÉśµÄŌĄķ ”£
£Ø2£©ŌŁÉś×°ÖĆÖŠ²śÉśµÄCO2ŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ӧɜ³É¼×“¼µČ²śĪļ£¬¹¤ŅµÉĻĄūÓĆøĆ·“Ó¦ŗĻ³É¼×“¼”£
ŅŃÖŖ£ŗ25 ”ę£¬101 KPaĻĀ£ŗ
H2(g) + 1/2 O2(g) === H2O(g) ¦¤ H1= -242 kJ/mol
CH3OH(g) + 3/2 O2(g) === CO2 (g) + 2 H2O(g) ¦¤ H2= -676 kJ/mol
¢Ł Š“³öCO2ŗĶH2Éś³ÉĘųĢ¬¼×“¼µČ²śĪļµÄČČ»Æѧ·½³ĢŹ½ ”£
¢Ś ĻĀĆę±ķŹ¾ŗĻ³É¼×“¼µÄ·“Ó¦µÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£¬ĘäÖŠÕżČ·µÄŹĒ £ØĢī×ÖÄøŠņŗÅ£©”£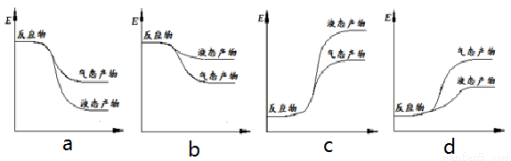
£Ø3£©ŌŚĆܱյÄŌŁÉś×°ÖĆÖŠ£¬¼ÓČė5 mol H2Óė2 mol CO2·¢Éś·“Ӧɜ³É¼×“¼£¬·“Ó¦“ļµ½Ę½ŗāŹ±£¬øıäĪĀ¶Č(T)ŗĶŃ¹Ēæ(P)£¬·“Ó¦»ģŗĻĪļÖŠ¼×“¼(CH3OH)µÄĪļÖŹµÄĮæ·ÖŹż±ä»ÆĒéæöČēĻĀĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A£®P1> P2> P3>P4
B£®¼×“¼µÄĪļÖŹµÄĮæ·ÖŹżŌ½øߣ¬·“Ó¦µÄĘ½ŗā³£ŹżŌ½“ó
C£®Ķ¼Ź¾ÖŠ£¬øĆ·“Ó¦µÄĪĀ¶Č±ä»ÆĪŖ£ŗT1> T2> T3>T4
D£®T4”¢P4”¢Ź±£¬H2µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ60%
£Ø4£©ŅŃÖŖijÖּד¼Č¼ĮĻµē³ŲÖŠ£¬µē½āÖŹČÜŅŗĪŖĖįŠŌ£¬Ź¾ŅāĶ¼ČēĻĀ£ŗ¹¤×÷½įŹųŗó£¬Bµē¼«ŹŅČÜŅŗµÄpHÓė¹¤×÷Ē°Ļą±Č½« £ØĢīŠ“”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£¬ČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©”£Aµē¼«ø½½ü¼×“¼·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖ ”£
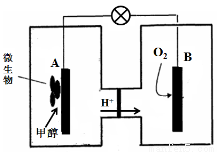
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ćĪ÷¹šĮÖ֊ѧø߶žÉĻĘŚÖŠæ¼ŹŌĄķ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
·Ö×ÓŹ½ĪŖC8H8O2µÄ·¼Ļć×å»ÆŗĻĪļ£¬ĘäÖŠŹōÓŚõ„ĄąµÄĶ¬·ÖŅģ¹¹ĢåÓŠ
A£®4ÖÖ B£®5ÖÖ C£®6ÖÖ D£®7ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«ÉīŪŚøß¼¶ÖŠŃ§øßŅ»ÉĻĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚĢå»żĻąĶ¬µÄĮ½øöĆܱÕČŻĘ÷ÖŠ·Ö±š³äĀśNO2”¢N2O4ĘųĢ壬µ±ÕāĮ½øöČŻĘ÷ÄŚĪĀ¶ČŗĶĘųĢåĆܶČĻąµČŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®Į½ÖÖĘųĢåµÄŃ¹ĒæĻąµČ B£®Į½ÖÖĘųĢåNŌ×ÓĪŖ1:2
C£®Į½ÖÖĘųĢåµÄ·Ö×ÓŹżÄæĻąµČ D£®Į½ÖÖĘųĢåµÄŃõŌ×ÓŹżÄæĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«¹ćÖŻÖ“ŠÅ֊ѧøßŅ»ÉĻĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹Ų½ŗĢåµÄŠšŹöÕżČ·µÄŹĒ
A£®½ŗĢåĮ£×ӵēóŠ”Ķس£ŌŚ0.1”«1nmÖ®¼ä
B£®Ńō¹ā“©ĶøĒå³æµÄŹ÷ĮÖŹ±ŠĪ³ÉµÄ¹āÖł£¬ŹĒ½ŗĢåµÄ¶”“ļ¶ūŠ§Ó¦µÄĢåĻÖ
C£®¼¦µ°ĒåČÜŅŗ·ÖĄąÉĻŹōÓŚŠü×ĒŅŗ
D£®ĻņFeCl3ČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬»į³öĻÖŗģŗÖÉ«Fe(OH)3½ŗĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«¹ćÖŻÖ“ŠÅ֊ѧø߶žÉĻĘŚÖŠĪÄ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ?????
»ÆѧÓėÉē»į”¢Éś»ī½ōĆÜĻąĮ¬”£ĻĀĮŠĖµ·ØŗĻĄķµÄŹĒ£Ø £©
A£®½ŚČÕĘŚ¼ä£¬ŌŚČĖČŗĆܼƓ¦Č¼·ÅŃĢ»Ø±¬Öń
B£®Ń°ÕŅŅ»ÖÖøߊ§“߻ƼĮ½«Ė®Ö±½Ó±ä³ÉĘūÓĶ
C£®³“²ĖŹ±ÓĶ¹ųÖŠµÄÓĶ²»É÷×Å»š£¬ŃøĖŁøĒÉĻ¹ųøĒ
D£®ÓƵćČ¼µÄ»š²ńŌŚŅŗ»ÆĘųøÖĘææŚ¼ģŃéŹĒ·ńĀ©Ęų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½ĮŁŗ£ĢØ֯֊ѧøßČżÉĻѧʌµŚČż“ĪĶ³Į·»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĢõ¼žĻĀŗĻ³ÉŅŅĻ©£ŗ 6H2(g) +2CO2(g)  CH2£½CH2(g) +4H2O(g)£»ŅŃÖŖĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹŗĶ“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°ĻģČēĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
CH2£½CH2(g) +4H2O(g)£»ŅŃÖŖĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹŗĶ“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°ĻģČēĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. Éś³ÉŅŅĻ©µÄĖŁĀŹ£ŗv(M)Ņ»¶ØŠ”ÓŚv(N)
B. »ÆŃ§Ę½ŗā³£Źż£ŗKN£¾K M
C. µ±ĪĀ¶ČøßÓŚ250”ꏱ£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬“Ó¶ųŹ¹“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶ
D£®ČōĶ¶ĮĻ±Čn£ØH2£©£ŗn£ØCO2£©=3£ŗ1£¬ŌņĶ¼ÖŠMµćŹ±£¬ŅŅĻ©µÄĢå»ż·ÖŹżĪŖ7.7£„
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓÄĻŹ”ø߶ž12ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻÖÓŠ1 L 0£®5mol/LµÄĮņĖįÄĘČÜŅŗ£¬ÓŠ¹ŲČÜŅŗµÄŠšŹöÕżČ·µÄŹĒ
A£®Č”0£®5 LČÜŅŗ£¬Na+µÄÅØ¶ČŹĒ0£®5 mol/L
B£®Č”0£®1 LČÜŅŗĻ”ŹĶÖĮl L£¬SO42-Ąė×ÓÅØ¶ČŹĒ0£®05 mol/L
C£®ČÜÖŹµÄĄė×Ó×ÜŹżŹĒ6£®02”Į1023øö
D£®øĆČÜŅŗŹĒ°Ń0£®5 mol Na2SO4ČÜÓŚ1 LĖ®ÖŠÅäÖʶų³ÉµÄ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com