
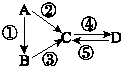
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:分析 (1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质,则A为S,C为SO2,B为H2S,D为SO3;
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染,判断为NO、NO2,B与C在一定条件下反应生成的A是大气主要成分,推断A为N2,B为NH3,C为NO、D为NO2;
(3)若A是太阳能电池用的光伏材料,B可用于制造光导纤维,则A为Si,B为Na2SiO3,C、D为钠盐,且D是厨房中常用的物质,则C为Na2SiO3、D为Na2CO3.
解答 解:(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质,则A为S,C为SO2,B为H2S,D为SO3,二氧化硫的用途:漂白、杀菌、消毒、作为硫酸的原料等,
故答案为:漂白、杀菌、消毒、作为硫酸的原料等;
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染,判断为NO、NO2,B与C在一定条件下反应生成的A是大气主要成分,推断A为N2,B为NH3,C为NO、D为NO2,B与C在一定条件下反应的化学方程式:4NH3+6NO$\frac{\underline{\;一定条件\;}}{\;}$5N2+6H2O,
故答案为:4NH3+6NO$\frac{\underline{\;一定条件\;}}{\;}$5N2+6H2O;
(3)若A是太阳能电池用的光伏材料,B可用于制造光导纤维,则A为Si,B为Na2SiO3,C、D为钠盐,且D是厨房中常用的物质,则C为Na2SiO3、D为Na2CO3,则C的电离方程式:Na2SiO3═2Na++SiO32-,④反应的化学方程式:Na2SiO3+CO2+H2O═Na2CO3+H2SiO3↓,
故答案为:Na2SiO3═2Na++SiO32-;Na2SiO3+CO2+H2O═Na2CO3+H2SiO3↓.
点评 本题考查了无机物的推断,涉及硫、氮、硅元素单质及其化合物,熟练掌握物质的性质与应用,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成 n mol A2,同时生成 n mol AB | |
| B. | 体系内的总压不随时间变化 | |
| C. | 单位时间内生成2n mol AB的同时生成n mol B2 | |
| D. | 单位时间内生成 n mol A2的同时,生成n mol B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与盐酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子的电子层数多 | |
| C. | 参与反应时1 mol A失去的电子比1 mol B失去的电子多 | |
| D. | 常温时,A能从盐酸中置换出氢气,而B不能反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是用来衡量微观粒子多少的一种物理量 | |
| B. | 1mol任何粒子的粒子数叫阿伏加德罗常数 | |
| C. | 若气体摩尔体积为22.4 L•mol-1,则所处条件为标准状况 | |
| D. | 常温下,将4gNaOH溶于100mL水中得到溶质浓度1mol/L的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
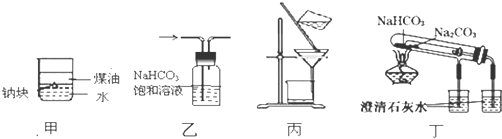
| A. | 用甲图装置证明密度ρ(煤油)<ρ(钠)<ρ(水) | |
| B. | 用乙图装置除去CO2中的HCl | |
| C. | 用丙图装置分离二氧化锰和氯化钠溶液 | |
| D. | 用丁图装置比较NaHCO3和Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com