
 |  |
| A.向100mL 0.1mol•L-1H2SO4溶液中滴加 0.1mol•L-1Ba(OH)2溶液至过量 | B.向100mL 0.1mol•L-1H2SO4溶液中加入NaOH固体 |
 |  |
| C.向一定浓度的氯化钠溶液中加水 | D.向蒸馏水中通入HCl气体 |
| A. | A | B. | B | C. | C | D. | D |
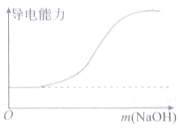
分析 水溶液要想导电必须具有自由移动的带电微粒,带电微粒越多越容易导电,据此进行分析;
A.向H2SO4溶液中滴加Ba(OH)2溶液至过量,由于发生了反应Ba(OH)2+H2SO4=BaSO4↓+2H2O,随着Ba(OH)2溶液的滴加,离子的浓度逐渐降低,导电能力逐渐降低,最后导电能力为0,也就是说恰好完全反应没有自由移动的离子,再滴加Ba(OH)2溶液,离子的浓度逐渐增加,导电能力逐渐增加;
B.向H2SO4溶液中加NaOH固体,由于发生了反应2NaOH+H2SO4=Na2SO4↓+2H2O,离子的浓度不变,故导电能力不变,最后导电能力为0,再加NaOH,离子的浓度逐渐增加,导电能力逐渐增加;
C.向一定浓度的氯化钠溶液中加水,氯化钠的浓度越来越小,故导电能力越来越小,但不为0;
D.向蒸馏水中通入HCl气体,刚开始无自由移动离子,故导电能力为0,随着HCl气体的通入,离子的浓度逐渐增加,导电能力逐渐增加.
解答 解:A.向H2SO4溶液中滴加Ba(OH)2溶液至过量,由于发生了反应Ba(OH)2+H2SO4=BaSO4↓+2H2O,随着Ba(OH)2溶液的滴加,离子的浓度逐渐降低,导电能力逐渐降低,最后导电能力为0,也就是说恰好完全反应没有自由移动的离子,再滴加Ba(OH)2溶液,离子的浓度逐渐增加,导电能力逐渐增加,故图象最低点为0与x轴相切,故A错误;
B.向H2SO4溶液中加NaOH固体,由于发生了反应2NaOH+H2SO4=Na2SO4↓+2H2O,离子的浓度不变,故导电能力不变,最后导电能力为0,再加NaOH,离子的浓度逐渐增加,导电能力逐渐增加,故B正确;
C.向一定浓度的氯化钠溶液中加水,氯化钠的浓度越来越小,故导电能力越来越小,但不为0,故C正确;
D.向蒸馏水中通入HCl气体,刚开始无自由移动离子,故导电能力为0,随着HCl气体的通入,离子的浓度逐渐增加,导电能力逐渐增加,故D正确;
故选A.
点评 本题属于图象题,解题的关键是知道水溶液要想导电必须具有自由移动的带电微粒,带电微粒越多越容易导电,本题难度中等.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
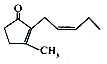
| A. | 茉莉酮易溶于水 | |
| B. | 茉莉酮中含有两种官能团 | |
| C. | 茉莉酮可与溴水、酸性KMnO4溶液发生加成反应,现象均为褪色 | |
| D. | 茉莉酮与二氢茉莉酮 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=2 mol•L-1•min-1 | B. | v(B)=1.2 mol•L-1•s-1 | ||
| C. | v(D)=0.4 mol•L-1•min-1 | D. | v(C)=0.1 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗分离乙醇和乙酸乙酯的混合物 | |
| B. | 新制氯水或浓硝酸存放在带橡皮塞的棕色玻璃瓶中 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 加热蒸发NaCl溶液时应用玻璃棒不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
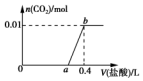 向NaOH和Na2CO3混合溶液中滴加0.1mol•L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是 ( )
向NaOH和Na2CO3混合溶液中滴加0.1mol•L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是 ( )| A. | 在0~a范围内,只发生NaOH和HCl的反应 | |
| B. | ab段发生反应的离子方程式为:CO32-+2H+═CO2↑+H2O | |
| C. | a=0.3 | |
| D. | 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
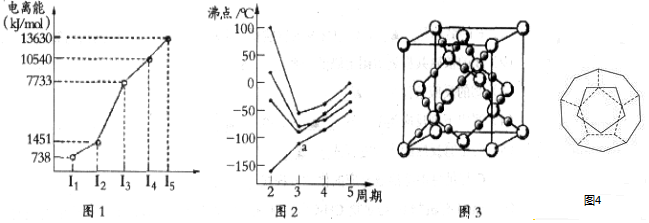
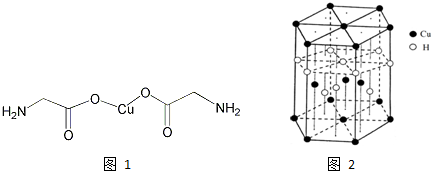
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com