
| A. | CS2是极性键构成的极性分子 | |
| B. | SO2与CO2为等电子体 | |
| C. | 金属晶体的六方最密堆积和面心立方最密堆积的方式空间利用率最高 | |
| D. | NaCl和CsCl的化学式相同,所以晶胞特点也是相同的 |
分析 A、CS2为非极性分子;
B、原子总数相同、电子总数或价电子总数相同的互为等电子体;
C、六方最密堆积和面心立方最密堆积空间利用率均为74%;
D、NaCl中阴阳离子配位数是6、CsCl中阴阳离子配位数是8.
解答 解:A、CS2含有极性键,空间结构为直线型,属于非极性分子,故A错误;
B、SO2与CO2的原子数相同,电子数和价电子数都不同,所以不是等电子体,故B错误;
C、简单立方堆积空间利用率为52%,体心立方堆积空间利用率68%,六方最密堆积和面心立方最密堆积空间利用率均为74%,所以金属晶体的六方最密堆积和面心立方最密堆积的方式空间利用率最高,故C正确;
D、NaCl、CsCl晶体的空间结构不相似,NaCl中阴阳离子配位数是6、CsCl中阴阳离子配位数是8,故D错误;
故选C.
点评 本题考查分子空间构型判断、等电子体,晶体结构等知识点,侧重考查学生分析判断能力,题目难度不大.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
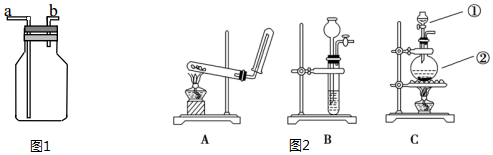
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol | B. | 4mol | C. | 6mol | D. | 8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | Li | C | N | O | F | Ne | ||
| 三 | Na | Mg | S | Cl | ||||
| 四 | K | Ca | Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烯的结构式:H2C=CHCl | B. | S2-的结构示意图: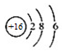 | ||
| C. | 熟石膏的化学式:2CaSO4•H2O | D. | 二氧化碳的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰气化 | B. | O2转变成O3 | C. | 加热NH4HCO3 | D. | 加热NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
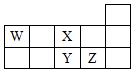
| A. | Z、Y、X的原子半径依次减小,非金属性依次降低 | |
| B. | Z、Y、W的最高价氧化物对应水化物的酸性依次降低 | |
| C. | WH4与Z元素的单质在一定条件下可能发生化学反应 | |
| D. | W的位置是第2周期、第ⅣA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com