
【题目】(1)已知氢有3种常见原子:11H、21H、31H(或H、D、T),氯有2种常见核素原子:35Cl、37Cl,氯气与氢气形成的氯化氢分子的相对分子质量有________种。
(2)质量相同的H216O和D216O所含质子数之比为______,中子数之比为________,电解产生的氢气在同温同压下体积之比为________,质量之比为________。
(3)2 g AO32-电子数比质子数多3.01×1022个,则A的相对原子质量为__________。
【答案】5 10∶9 8∶9 10∶9 5∶9 32
【解析】
(1)根据排列组合可知,写出可能形成的氯化氢的分子组成;
(2)利用分子组成及分子中质量数等相关数据进行计算;
(3)根据电荷等数据进行分析计算。
(1)氯化氢有H35Cl、H37Cl、D35Cl、D37Cl、T35Cl、T37Cl;但H37Cl与T35Cl的相对分子质量相同,所以相对分子质量有5种;
(2)设质量都为1 g,H216O与D216O的质子数之比为![]() ×10)∶(
×10)∶(![]() ×10)=10∶9,中子数之比为(
×10)=10∶9,中子数之比为(![]() ×8)∶(
×8)∶(![]() ×10)=8∶9,电解产生的氢气在同温同压下的体积比,即物质的量之比为
×10)=8∶9,电解产生的氢气在同温同压下的体积比,即物质的量之比为![]() ∶
∶![]() =10∶9,质量比为(
=10∶9,质量比为(![]() ×2)∶(
×2)∶(![]() ×4)=5∶9。
×4)=5∶9。
(3)多出来的电子数就是离子所带的电荷数。
AO32- ~ 电子数比质子数多的数目
[48+Ar(A)] g·mol-1 2×6.02×1023 mol-1
2 g 3.01×1022
得Ar(A)=32。


科目:高中化学 来源: 题型:
【题目】通过加入适量乙酸钠,设计成微生物电池可以将废水中的氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是
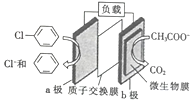
A. b极为正极,发生还原反应
B. 一段时间后b极区电解液的pH减小
C. H+由a极穿过质子交换膜到达b极
D. a极的电极反应式为![]() -e-=Cl-+
-e-=Cl-+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.100 mL 0.1 mol·L-1的稀硫酸中含有SO42-个数为0.1NA
B.常温常压下,4 g氦气所含有的中子数为4NA
C.2.7 g金属铝与足量的盐酸反应,铝失去电子数为3NA
D.12.4 g白磷(分子式为P4)中含有磷原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2.3 g钠投入足量水中,充分反应后所得溶液用水稀释至100 mL。求:
(1)生成标准状况下的氢气多少升_______;
(2)所得的溶液物质的量浓度_______?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.![]()
B. Al![]() NaAlO2
NaAlO2![]() Al(OH)3
Al(OH)3
C. Fe![]() FeCl2
FeCl2![]() FeCl3
FeCl3
D. Na![]() Na2O
Na2O![]() NaOH
NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在水槽![]() 中装有
中装有![]() 水,容积为
水,容积为![]() 的试管
的试管![]() 中充满了
中充满了![]() 和
和![]() 的混合气体(标准状况下),将试管
的混合气体(标准状况下),将试管![]() 倒插入水槽
倒插入水槽![]() 中。充分反应后,试管
中。充分反应后,试管![]() 中剩余气体的体积为
中剩余气体的体积为![]() 。
。
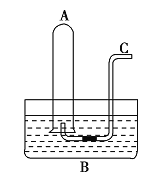
(1)将![]() 倒插入水槽
倒插入水槽![]() 中发生的反应为________________________________________________,该反应中氧化剂与还原剂的质量比为_____________;原混合气体中
中发生的反应为________________________________________________,该反应中氧化剂与还原剂的质量比为_____________;原混合气体中![]() 与
与![]() 的物质的量之比为____________。
的物质的量之比为____________。
(2)通过导气管![]() 向剩余
向剩余![]() 气体的试管
气体的试管![]() 中持续通入氧气,
中持续通入氧气,![]() 中可能观察到的现象是_____________________________________________________________________________________________________。
中可能观察到的现象是_____________________________________________________________________________________________________。
(3)当试管![]() 中充满气体时停止通入氧气,然后将试管从水槽中取出,水槽
中充满气体时停止通入氧气,然后将试管从水槽中取出,水槽![]() 中溶液的物质的量浓度为______
中溶液的物质的量浓度为______![]() (设水槽中液体的体积仍为
(设水槽中液体的体积仍为![]() )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)已知Se在周期表的位置为_____,基态Ga原子核外电子占据的最高能级为_____。
(2)P、S、Ga电负性从大到小的顺序为_____。
(3)与Al元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为____(标出配位键)
(4)已知[Cu(H2O)4]2+具有对称的空间构型,[Cu(H2O)4]2+中的2个H2O被Cl-取代,能得到2种不同结构的产物,则[Cu(H2O)4]2+的空间构型为_____。请画出该离子中配位键的结合形式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及铝的化合物有着极为广泛的用途。
(1)金属铝的生产是以Al2O3为原料,在熔融状态下用石墨做阴极和阳极进行电解:
2Al2O3![]() 4Al+3O2↑,则电解时不断消耗的电极是_____(填“阳极”或“阴极”)
4Al+3O2↑,则电解时不断消耗的电极是_____(填“阳极”或“阴极”)
(2)铝片、石墨、空气和海水构成的原电池可用于航标供电,该原电池正极的电极反应是_____。
(3)泡沫灭火器中NaHCO3溶液和Al2(SO4)3溶液发生反应的离子方程式是______。
(4)在配制AlCl3溶液时,防止溶液出现浑浊现象,溶液中应加入_____。
(5)Mg(OH)2固体能除去镁盐溶液中Al3+,原因是_____。(用离子方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com