
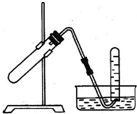
 如图所示装置可用于
如图所示装置可用于 Na2CO3+H2O+CO2↑,因固体药品中有湿存水,试管口应向下倾斜,CO2能溶于水,不能用排水法收集,故A错误;
Na2CO3+H2O+CO2↑,因固体药品中有湿存水,试管口应向下倾斜,CO2能溶于水,不能用排水法收集,故A错误; Na2SO4+2HCl,需加热与图中的装置无需加热矛盾,生成的气体氯化氢极易溶于水,不能用排水法收集,所以不能用该装置制氯化氢,故D错误;
Na2SO4+2HCl,需加热与图中的装置无需加热矛盾,生成的气体氯化氢极易溶于水,不能用排水法收集,所以不能用该装置制氯化氢,故D错误;

科目:高中化学 来源: 题型:
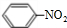
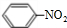
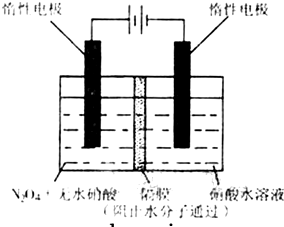
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:
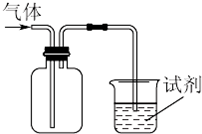 如图所示装置可用于收集气体并验证其某些化学性质,你认为正确的是
如图所示装置可用于收集气体并验证其某些化学性质,你认为正确的是| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | NH3 | 酚酞试液 | 溶液变红色 | NH3的水溶 液显碱性 |
| B | NO2 | KI淀粉溶液 | 溶液变蓝 | NO2的水溶 液有氧化性 |
| C | X | 澄清石灰水 | 溶液变浑浊 | X是CO2 |
| D | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性 和漂白性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
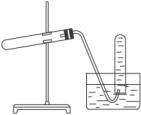
A.加热NaHCO3制CO2
B.用Cu与稀HNO3反应制NO
C.用NH4Cl与浓NaOH溶液反应制NH3
D.用MnO2与浓盐酸反应制Cl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com