
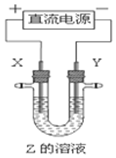
| A. | 氯碱工业中,X、Y均为石墨,Y附近能得到氢氧化钠 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 电镀工业中,X是待镀金属,Y是镀层金属 | |
| D. | 外加电流的阴极保护法中,X是待保护金属 |
分析 A.氯碱工业上,用惰性电极电解饱和氯化钠溶液,阳极上析出氯气,阴极上析出氢气,阴极附近得到氢氧化钠;
B.铜的精炼中,粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解质溶液;
C.电镀工业上,镀层作阳极,镀件作阴极;
D.外加电流的阴极保护法中,阴极是待保护金属.
解答 解:A.氯碱工业上,用惰性电极电解饱和氯化钠溶液,阴极附近得到氢氧化钠,即Y附近能得到氢氧化钠,故A正确;
B.铜的精炼中,粗铜作阳极X,纯铜作阴极Y,硫酸铜溶液作电解质溶液,故B错误;
C.电镀工业上,Y是待镀金属,X是镀层金属,故C错误;
D.外加电流的阴极保护法中,阴极是待保护金属,即Y铁是待保护金属不溶解,故D错误.
故选A.
点评 本题考查了电解原理,根据电解时离子的放电顺序、电镀、电解精炼、金属的腐蚀与防护来分析解答即可,难度不大,注意原电池原理和电解池原理是高考的热点,应掌握此知识点.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 为该转化过程的催化剂
为该转化过程的催化剂查看答案和解析>>
科目:高中化学 来源: 题型:选择题
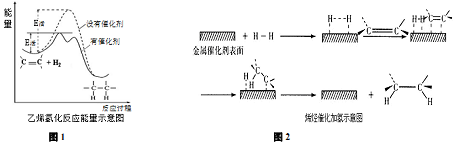
| A. | 乙烯和H2生成乙烷的反应△H>0 | |
| B. | 加入催化剂,降低了E活,并减小了反应的△H | |
| C. | 图1表明,催化加氢过程中催化剂参与反应过程并形成不稳定的中间体 | |
| D. | 图2表明,催化加氢过程中催化剂将较难发生的反应分成了多个容易发生的反应,可提高反应物的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液).下列说法中不正确的是( )
为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液).下列说法中不正确的是( )| A. | 石墨电极作正极,发生还原反应 | |
| B. | 铂电极的电极反应式为:C8H18+16H2O-50e-═8CO2+50H+ | |
| C. | 每消耗标准状况下5.6 L O2溶液中通过lmol 电子 | |
| D. | H+由质子交换膜左侧向右侧迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )| 选项 | W | X |
| A | 稀硫酸 | Na[Al(OH)4]溶液 |
| B | 稀硝酸 | Fe |
| C | CO2 | Ca(OH)2溶液 |
| D | Cl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
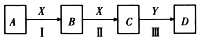
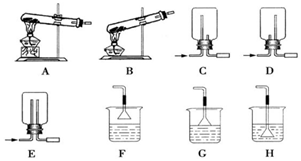
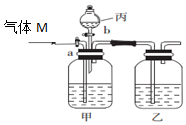
| A.气体M是SO2和H2的混合物 | B.气体M是SO2和H2的体积比为4:1 |
| C.反应中共消耗锌97.5g | D.反应中共转移电子3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HCl>H2S>PH3 | |
| B. | 若离子半径:R2->M+,则原子序数一定:R>M | |
| C. | 酸性强弱:H2SiO3<H2CO3<CH3COOH | |
| D. | 熔点:金刚石>食盐>干冰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com