
向某FeBr2溶液中通入1.12 L(标准状况)的Cl2,测得溶液中c(Br-)=3c(Cl-)=0.3 mol·L-1。反应过程中溶液的体积变化不计。则下列说法中正确的是 ( )。
A.原溶液的浓度为0.1 mol·L-1
B.反应后溶液中c(Fe3+)=0.1 mol·L-1
C.反应后溶液中c(Fe3+)=c(Fe2+)
D.原溶液中c(Br-)=0.4 mol·L-1
解析 该题解题的关键是明确Cl2与Fe2+和Br-的反应顺序。还原性Fe2+>Br-,向FeBr2溶液中通入Cl2时,反应顺序为2Fe2++Cl2===2Fe3++2Cl-、2Br-+Cl2===Br2+2Cl-,测得溶液中含有Br-,说明Cl2完全反应转化为Cl-,1.12 L(标准状况)Cl2的物质的量为0.05 mol,根据氯原子守恒可知n(Cl-)=0.1mol,则溶液的体积为1 L,溶液中n(Br-)=3n(Cl-)=0.3 mol。若溶液中Br-参加反应,令溶液中FeBr2物质的量为x mol,则根据电子转移守恒,x+(2x-0.3)=0.1,解得x=2/15 mol,2/15 mol Fe2+的提供电子为2/15 mol大于0.05 mol Cl2能够获得电子0.1 mol,且(2x-0.3)<0,不符合题意。若溶液中Br-未参加反应,则原溶液中的Fe2+物质的量为0.15 mol,0.15 mol Fe2+能够提供电子 0.15 mol,0.05 mol Cl2能够获得电子 0.1 mol,Fe2+有剩余,符合题意,所以原溶液含有FeBr2 0.15 mol,根据电子转移守恒,被氧化的Fe2+为0.05 mol×2=0.1 mol,生成Fe3+为0.1 mol,剩余Fe2+为0.15 mol-0.1 mol=0.05 mol。A项,原溶液含有FeBr2 0.15 mol,则原溶液的浓度为 0.15 mol·L-1,错误;B项,反应后溶液中生成的Fe3+为0.1 mol,则反应后溶液中c(Fe3+)=0.1 mol·L-1,正确;C项,反应后溶液中c(Fe2+)=0.05 mol·L-1,错误;D项,原溶液中含有FeBr2 0.15 mol,则原溶液中c(Br-)=0.3 mol·L-1,错误。
答案 B


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
现有含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是(离子形成沉淀或沉淀的溶解与溶液pH的关系如下表) ( )。
| 离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
| 开始沉淀时的pH | 8.93 | 3.56 | 开始溶解时的pH | 8.04 |
| 完全沉淀时的pH | 10.92 | 4.89 | 完全溶解时的pH | 12.04 |

查看答案和解析>>
科目:高中化学 来源: 题型:
向含有a mol AlCl3的溶液中加入含b mol KOH的溶液,生成沉淀的物质的量可能是 ( )。
①a mol ②b mol ③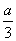 mol ④
mol ④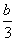 mol ⑤0 mol ⑥(4a-b) mol
mol ⑤0 mol ⑥(4a-b) mol
A.①②④⑥ B.①③④⑤⑥
C.②③⑤⑥ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取可以通过如下反应完成:Na+NaNO3 Na2O+N2↑(未配平)。请回答下列问题:
Na2O+N2↑(未配平)。请回答下列问题:
(1)上述反应的氧化剂是________(写化学式)。制取Na2O时,若金属钠与NaNO3按质量比23∶17投料,充分反应后收集到的气体体积为1.12 m3(标准状况下),则制得的Na2O的质量为________ kg。
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。

可选用的试剂:
a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液
e.酚酞 f.碱石灰 g.稀盐酸
| 实验过程中发生反应的化学方程式 | 实验所需仪器(用字母表示) | 实验所需试剂(用字母表示) | 实验需直接测定的有关物理量(用文字说明) |
(3)某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下:




该Na2O产品中Na2O的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
O3具有强氧化性,将O3通入KI溶液中发生反应:O3+I-+H+―→I2+O2+H2O(未配平),下列说法正确的是 ( )。
A.配平后的离子方程式为2O3+2I-+4H+===I2+2O2+2H2O
B.每生成1 mol I2转移电子2 mol
C.O2是还原产物之一
D.该反应能说明O2的氧化性大于I2的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.根据1H核磁共振谱图可以推知有机物分子中有几种不同类型的氢原子
B.红外光谱是用高能电子流等轰击样品分子,使分子失去电子变成分子、离子或碎片离子
C.元素分析仪具有快速、微量、精确等特点
D.通过红外光谱可以测知有机物所含的官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
在阿司匹林的结构简式中①②③④⑤⑥分别标出了其分子中的不同的键。将阿司匹林与足量NaOH溶液共煮时,发生反应时断键的位置是( )
A.①④ B.②⑤
C.③⑤ D.②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在某一溶液中,含有NH+4、I—、Ba2+、Cl—等离子,则该溶液的pH和介质可以是
A.pH=12,氨水为介质 B.pH=8,次氯酸钠溶液为介质
C.pH=3,H2SO4溶液为介质 D.pH=l,稀硝酸为介质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.0.1 mol·L-1NH4Cl溶液:c(NH4+)=c(Cl-)
B.在25℃时,pH=4的盐酸与pH=10的氨水溶液等体积混合后pH>7
C.0.1 mol·L-1与0.2 mol·L-1氨水溶液中c(OH-)之比为1︰2
D.中和pH与体积都相同的氨水和Ba(OH)2溶液,消耗HCl的物质的量之比是1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com