
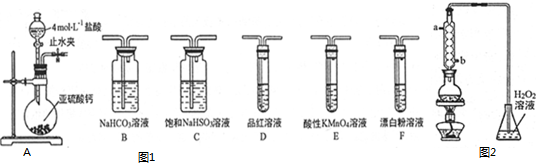
分析 (1)二氧化硫与氢硫酸反应生成硫,反应中二氧化硫表现氧化性;
(2)①按照A→C→F顺序连接装置,其中饱和的亚硫酸氢钠除去HCl,二氧化硫通入次氯酸钙溶液发生了氧化还原反应;
②次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强碱性判断.A装置制备二氧化硫,由于盐酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠除去HCl,再通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中的二氧化硫,用品红溶液检验二氧化碳中二氧化硫是否除尽,再通入F中;
(3)①采取逆流原理通入冷凝水;
②根据关系式:SO2~H2SO4~2NaOH计算.
解答 解:(1)二氧化硫与氢硫酸反应生成硫,反应中二氧化硫表现氧化性,利用装置1中产生的气体证明+4价硫具有氧化性:将SO2通入氢硫酸溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性,
故答案为:将纯净的SO2通入氢硫酸溶液溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性;
(2)①按照A→C→F顺序连接装置,其中饱和的亚硫酸氢钠除去HCl,二氧化硫通入次氯酸钙溶液发生了氧化还原反应,不能证明强酸制备弱酸的原理,不能证明亚硫酸和次氯酸的酸性强弱,
故答案为:二氧化硫通入次氯酸钙溶液发生了氧化还原反应不能证明强酸制备弱酸的原理;
②次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强碱性判断.A装置制备二氧化硫,由于盐酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠除去HCl,再通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中的二氧化硫,用品红溶液检验二氧化碳中二氧化硫是否除尽,再通入F中,则装置连接顺序为A、C、B、E、D、F,其中装置C的作用是除去HCl气体,D中品红不褪色,F中出现白色沉淀,可证明亚硫酸的酸性强于次氯酸,
故答案为:B、E;除去HCl气体以免影响后面的实验测得;装置D中品红不褪色,F中出现白色沉淀;
(3)①采取逆流原理通入冷凝水,即球形冷凝管进水口为b,
故答案为:b;
②设残液中SO2含量为xg.L-1,则:
SO2~~H2SO4~~2NaOH
64g 2mol
xg.L-1×0.001L 0.02L×0.1mol/L
所以64g:xg.L-1×0.001L=2mol:0.02L×0.1mol/L
解得x=64.00
故答案为:64.00.
点评 本题考查气体制备与性质实验、物质含量测定实验,涉及装置分析与评价、实验方案设计、仪器使用、化学计算等,关键是明确实验原理,较好的考查学生实验综合能力与知识迁移应用,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 次数 | 第1次 | 第2次 |
| 加入稀盐酸的质量/g | 50 | 50 |
| 剩余固体的质量/g | 2.6 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (c-a-b)kJ | B. | (a+b-c)kJ | C. | (2c-a-b)kJ | D. | $\frac{2c-a-b}{2}$kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应CH4+H2O $\frac{\underline{催化剂}}{△}$3H2+CO,每消耗1 mol CH4转移12 mol电子 | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-═2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 电极B上发生的电极反应为:O2+2CO2+4e-═2CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
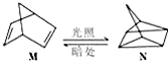 △H=+88.6kJ/mol
△H=+88.6kJ/mol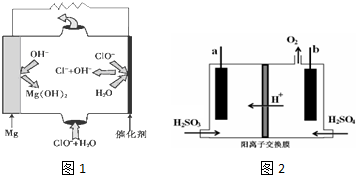
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com