
| A. | 钠跟水 | B. | 氧化钠跟水 | C. | 过氧化钠跟水 | D. | 电解水 |
分析 含元素化合价变化的反应为氧化还原反应,水中H、O元素的化合价不变,则水既不是氧化剂又不是还原剂,以此来解答.
解答 解:A.Na元素的化合价升高,水中H元素的化合价降低,则水为氧化剂,故A不选;
B.反应生成NaOH,没有元素的化合价变化,不属于氧化还原反应,故B不选;
C.过氧化钠中O元素的化合价变化,为氧化还原反应,水中H、O元素的化合价不变,则水既不是氧化剂又不是还原剂,故C选;
D.生成氢气、氧气,水中H、O元素的化合价均变化,则水既是氧化剂又是还原剂,故D不选;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断及迁移应用能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2A+3B=2C | B. | A+3B=2C | C. | 3A+B=2C | D. | A+B=C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 、G的结构式为O=C=O;若向M溶液通入G否(是或否)有沉淀,若再通入足量E观察到的现象是有白色沉淀.
、G的结构式为O=C=O;若向M溶液通入G否(是或否)有沉淀,若再通入足量E观察到的现象是有白色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
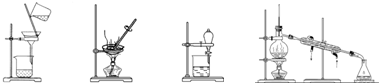
| A. | 蒸发、蒸馏、过滤、萃取 | B. | 过滤、蒸馏、蒸发、萃取 | ||
| C. | 过滤、蒸发、分液、蒸馏 | D. | 萃取、蒸馏、蒸发、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题



 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3,3-二甲基-1-丁烯在一定条件下与氢气充分反应后得到3,3-二甲基丁烷 | |
| B. | 工业生产中用乙醇与氢氧化钠作用生成乙醇钠,故乙醇可以与氢氧化钠溶液反应 | |
| C. | 地球上最基本的能源是太阳能,植物通过光合作用吸收太阳能,被吸收的太阳能通过各种形式的化学反应转化为化学能,物质中的化学能又可以通过各种形式的化学反应转化为热能、光能或电能 | |
| D. | 道尔顿、汤姆生、卢瑟福、波尔和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氧化性由强到弱的顺序:X3+>Cu2+>H+ | |
| B. | 金属X可能为Al | |
| C. | 据图判断,金属X能与稀硫酸反应产生H2 | |
| D. | 通过电子的物质的量大于0.3mol时,发生反应的化学方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 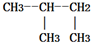 与 与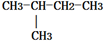 | B. | CH2=CH2与CH-CH3 | ||
| C. | 氢H和重氢D(${\;}_{1}^{1}$H与${\;}_{1}^{2}$H) | D. | 氧气与臭氧(O3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com