
| �ʰ��ᣨNH2CH2COOH�� | ������ | �ʰ������� |
| ������ˮ�������Ҵ������Ի����� | ������ˮ���Ҵ�����ǿ���Ժͻ�ԭ�� | ������ˮ���������Ҵ� |
| ʵ�� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| ��ϵpH | 4.0 | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 | 7.5 |
| ����/% | 65.74 | 74.96 | 78.78 | 83.13 | 85.57 | 72.98 | 62.31 | 5686�� |
���� ��1�����������н�ǿ�Ļ�ԭ�ԣ����Ʊ�̼�������Ĺ����У�Ҫ��ֹ��������������������������̼��������ӷ�Ӧ����̼����������
��2���ٷ�ֹ�ӷ���HCl���ź����ʵ�飬�����ȥ����ѡ�ñ���NaHCO3��Һ��
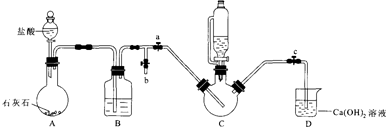
�ڵ�C�п����ž���Ӧֹͣ�μ����ᣬ�Ʊ������Ӳ�ر�ֹˮ��b����ֹˮ��a��
��װ��D��Ca��OH��2���������ж�װ���п����Ƿ��ž���
��pH����ʹ�����½���ԭ����H+����NH2CH2COOH�еİ�����Ӧ����������ǿ���Ժͻ�ԭ�ԣ����û��дٽ�FeCO3�ܽ⣬��ֹ��������������
�����ڸʰ�������������ˮ���������Ҵ������Ҵ��������ǽ��ʰ���������ˮ�е��ܽ�ȣ���߲��ʺʹ��ȣ�
����ԭ���غ㣬�̷��е���Ԫ��Ϊ0.10mol��������NH4HCO3��Һ�������ʸ�����ԭ���غ���㣬����=$\frac{ʵ�ʲ���}{���۲���}��100%$��
��3���ⶨ��Ʒ�ж�������������ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2-3�Σ��ɸ������ĵĸ�����ص������������������
��� �⣺��1�����������н�ǿ�Ļ�ԭ�ԣ����Ʊ�̼�������Ĺ����У�Ϊ�˷�ֹ��������������������������ۣ��̷���ˮ��Һ��NH4HCO3��Һ��Ӧ�ķ���ʽΪ Fe2++2HCO3-=FeCO3��+CO2��+H2O���ʴ�Ϊ����ֹ��������������Fe2++2HCO3-=FeCO3��+CO2��+H2O��
��2��������ϡ������ʯ�����Ʊ�������̼�Ĺ����У�HCl�лӷ��ԣ�Ϊ�˱���ӷ�����HCl���ź������飬�����ȥ����ѡ�ñ���NaHCO3��Һ���ʴ�Ϊ������NaHCO3��Һ��
�ڵ�C�п����ž���Ӧֹͣ�μ����ᣬ�Ʊ�����˹��̲���Ҫ������̼����Ҫ�����������ʲ��ܽ����Ҳ�ķ�Ӧװ�ã���Ӳ�ر�ֹˮ��b����ֹˮ��a���ʴ�Ϊ��b��a��
��װ��D��Ca��OH��2���������ж�װ���п����Ƿ��ž�����������������Ҫ�����������������ʵ����ɸ��ţ��ʴ�Ϊ���ж�װ���п����Ƿ��ž���
��pH����ʹ�����½���ԭ����H+����NH2CH2COOH�еİ�����Ӧ����������ǿ���Ժͻ�ԭ�ԣ����û��дٽ�FeCO3�ܽ⣬��ֹ���������������ʴ�Ϊ��H+����NH2CH2COOH��Ӧ��bc��
�����ڸʰ�������������ˮ���������Ҵ������Ҵ��������ǽ��ʰ���������ˮ�е��ܽ�ȣ���߲��ʺʹ��ȣ��ʴ�Ϊ�����ʰ���������ˮ�е��ܽ�ȣ���߲��ʺʹ��ȣ�
����ԭ���غ㣬�̷��е���Ԫ��Ϊ0.10mol��������NH4HCO3��Һ�������ʸ�����ԭ���غ�֪�����ϲ���[��NH2 CH2COO��2 Fe0.10mol��������Ϊ20.4g���ʲ���=$\frac{ʵ�ʲ���}{���۲���}��100%$=$\frac{m}{20.4}��100%$���ʴ�Ϊ��$\frac{m}{20.4}��100%$��
��3���ⶨ��Ʒ�ж�������������ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2-3�Σ��ɸ������ĵĸ�����ص�������������������ʴ�Ϊ����ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2-3�Σ�
���� ���⿼��ʵ���Ʊ��������漰��ѧ��Ӧ����ԭ�����Բ����ķ������ۡ����ʷ����ᴿ��������ԭ��Ӧ�ζ�Ӧ�õȣ���ȷԭ���ǽ���ؼ����Ƕ�ѧ���ۺ������Ŀ��飬��Ŀ�Ѷ��еȣ�


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���ͻ���� |
| A | �ýྻ��Ptպȡij��Һ������ɫ��Ӧ������ʻ�ɫ | ����Һ��һ������Na+����k+ |
| B | �ýྻ�IJ����������Na2O2����֬��������֬��ȼ�� | CO2��H2O��Na2O2��Ӧ�Ƿ��ȷ�Ӧ |
| C | ����ˮ�е���ֲ���ͣ����Ͳ�����ɫ | �岻������֬ |
| D | �������ữ��H2O2����Fe��NO3��2��Һ����Һ���ɫ | H2O2�������Ա�Fe3+ǿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 0.1 mol•L-1 CH3COONa��Һ��0.1 mol•L-1 CaCl2��Һ�������ϣ�c��Na+��+2c��Ca2+��=c��CH3COO-��+c��CH3COOH��+c��Cl-�� | |
| B�� | Ũ�Ⱦ�Ϊ0.1 mol•L-1��С�մ���Һ���ռ���Һ�������ϣ�c��OH-��-c��H+��=c��HCO3-��+c��H2CO3�� | |
| C�� | pH��ͬ�İ�ˮ��KOH��Һ��Ba��OH��2��Һ�У�c��NH4+��=c��K+��=2c��Ba2+�� | |
| D�� | �����£�0.2 mol•L-1 NH4NO3��Һ��0.1 mol•L-1 NaOH��Һ�������ϣ�����pH=9.6����Һ�У�c��NO3-����c��Na+����c��NH4+����c��NH3•H2O����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ�ú��ʵĴ������Լӿ췴Ӧ���� | |
| B�� | ����O2��Ũ�ȿ�ʹSO3��Ũ�ȼ�С | |
| C�� | �����¶ȿ��Լ�С��Ӧ���� | |
| D�� | ����SO2��Ũ�ȿ�������Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
�� ��
��
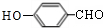 +Na2CO3��
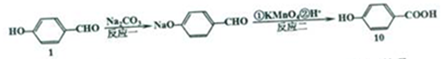
+Na2CO3��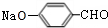 +NaHCO3����Ŀ���DZ������ǻ�����ֹΪ������
+NaHCO3����Ŀ���DZ������ǻ�����ֹΪ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢݢޢ� | B�� | �٢ڢۢޢ� | C�� | �٢ܢݢޢ� | D�� | �٢ڢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȼ���ֻ��һ�֣�˵���������������ṹ | |
| B�� | 2-��ϩ�ĸ�̼ԭ�ӹ�ƽ�棬˵����ϩ������ƽ��ṹ | |
| C�� | ����Ȳ����������ԭ�ӹ�ƽ�棬˵����Ȳ������ԭ����һ��ֱ���� | |
| D�� | �ڶ��ױ�ֻ��һ�֣�˵���������в����ڵ�˫�������̼̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ��K+��NO3-��OH-���Դ������� | |
| B�� | ����Һ�Լ��Ե�ԭ��ΪClO-+H2O?HClO+OH- | |
| C�� | �����Һ�е�������FeSO4��Һ����Ӧ�����ӷ���ʽΪ��2Fe2++ClO-+2H+�TCl-+2Fe3++H2O | |
| D�� | �����Һ�м���Ũ���ᣬÿ����1molCl2��ת�Ƶ���ԼΪ6.02��1023�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com