
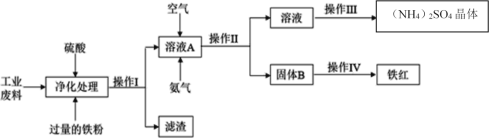
����Ŀ������������ָ��ԭ�Ͻ��л�ѧ�ӹ������ջ���м�ֵ�IJ�Ʒ���������̡�ij�о�С�����ú���������������ͭ�Ĺ�ҵ�����Ʊ�����(������)������茶��塣������ͼ��
��ش��������⣺
��1������I������_____�������������____��
��2�������ijɷ�Ϊ_____��
��3����д����ҺA�з�Ӧ�����ӷ���ʽ___���ڱ�״���£�ת��0.4NA������ʱ��ͨ��Ŀ������Ϊ_____��
��4���ⶨ����������ͭ��������������ȡag������Ʒ��������I�õ���������������ϡ�����ܽ⡢���ˡ�ϴ�ӡ�����Ƶù��������Ϊb g�������������ͭ����������____(д������ʽ)��
��5����ҵ������Һ�м������������Ը�����أ�д���йص����ӷ���ʽ___��
���𰸡����� ����Ũ������ȴ�ᾧ Fe��Cu 10H2O+8NH3+O2+4Fe2+��4Fe(OH)3��+8NH4+ 10.7L (5b/2a)��100% 5Fe2++MnO4-+8H+��5Fe3++Mn2++4H2O
��������
����������������ͭ�Ĺ�ҵ�����м��������ܽ⣬�������������������ͭ�����û���Ӧ�õ����ܵ�ͭ���ʣ����ˣ�����Ϊͭ��δ��Ӧ���������ҺAΪ������������Һ��������ͨ�����������������Ϊ�����ӣ����백�����������ӣ����ˣ�����BΪ������������ҺΪ�������Һ�����������Һ����Ũ������ȴ�ᾧ�õ�����茶��壬������B���������������յõ����������ݴ˽��
��1����������I�õ��������Һ���ʲ���IΪ���ˣ�������Ϊ���������Һ����Ũ����ȴ�ᾧΪ����茶��塣�ʴ�Ϊ�����ˣ�����Ũ������ȴ�ᾧ��
��2��ͨ�����������۽�����ͭ��ԭΪͭ���ʣ�������Ϊͭ��δ��Ӧ��������ʴ�Ϊ��Fe��Cu��
��3����ҺAΪ������������Һ��������ͨ�����������������Ϊ�����ӣ����백�����������ӣ����ˣ�����BΪ������������ҺΪ�������Һ����ҺA�з�Ӧ�����ӷ���ʽΪ10H2O+8NH3+O2+4Fe2+��4Fe(OH)3��+8NH4+�����ݷ�Ӧ����ʽ�ɵã�����1mol������ת��4mol���ӣ��ڱ�״���£�ת��0.4NA������ʱ����Ҫ����0.1mol�����������Ϊ2.24L�������ڿ����е��������Ϊ21%�����ͨ��Ŀ������Ϊ![]() ��10.7L����Ϊ��10H2O+8NH3+O2+4Fe2+��4Fe(OH)3��+8NH4+��10.7L��
��10.7L������10H2O+8NH3+O2+4Fe2+��4Fe(OH)3��+8NH4+��10.7L��
��4����ȡag������Ʒ������I�õ�������Ϊͭ��������������ϡ�����ܽ⡢���ˡ�ϴ�ӡ�����Ƶù��������Ϊbg��ͭ���ܽ⣬��m(Cu)��bg����n(Cu)=![]() mol������ͭԪ�������غ㣬��n(CuSO4)��n(Cu)=
mol������ͭԪ�������غ㣬��n(CuSO4)��n(Cu)=![]() mol�������������ͭ����������Ϊ
mol�������������ͭ����������Ϊ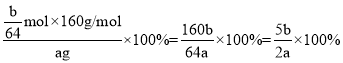 ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��5����ҵ���ϣ�����������������ͭ����Һ�м������������Ը�����أ��������������Ը�����ط���������ԭ��Ӧ�����ӷ���ʽΪ5Fe2++MnO4-+8H+��5Fe3++Mn2++4H2O���ʴ�Ϊ��5Fe2++MnO4-+8H+��5Fe3++Mn2++4H2O��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ���з���һ������Һ����ε�أ��乤��ԭ����ͼ��ʾ������˵���������
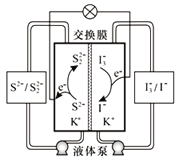
A. �ŵ�ʱ��������Ϊ����������������Ӧ
B. ���ʱ���������Һ��K+������Ĥ���Ҳ��ƶ�
C. �ŵ�ʱ������Ҳ�ĵ缫��ӦΪI3-+2e-=3I-
D. ���ʱ����ص��ܷ�ӦΪS22-+3I-![]() 2S2-+I3-
2S2-+I3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к���80����Ԫ�أ�����Ҫ��������Դ���⣬ͬʱ��ˮ����ǿ�����Ȼ����������Ϊ���������Ⱦ�����ṩ�˹����Ŀռ䡣
(1)����֪��ͬpH�����£�ˮ��Һ��̼Ԫ�صĴ�����̬����ͼ��ʾ��

����˵������ȷ����_____________ (����ĸ���)��
a. pH=8ʱ����Һ�к�̼Ԫ�ص�����Ҫ��HCO3��
b. A�㣬��Һ��H2CO3��HCO3��Ũ����ͬ
c. ��c(HCO3��)=c(CO32��)ʱ��c(H+)>c(OH��)
��������pH=8.4��ˮ��Һ�м���NaOH��Һʱ������Ӧ�����ӷ���ʽ��_____________��
(2)��ˮpH�ȶ���7.9��8.4֮�䣬�������̵�����CO2��SO2�����ռ���
�ٺ�ˮ�к��е�OH�����������̵����е�CO2��ͬʱΪ��ˮ�Ѹƣ�����CaCO3��д���˷�Ӧ�����ӷ���ʽ��_____________��
����֪��25��ʱ��H2CO3����ƽ�ⳣ��K1=4.3��10��7 K2=5.6��10��11
H2SO3����ƽ�ⳣ��K1=1.5��10��2 K2=6.0��10��8
��ˮ�к��е�HCO3������������SO2���ù��̲�������CO2��_____________��
(3)ϴ��������ĺ�ˮ�����ԣ��账���������ŷš������ʺ�ˮ���ͬʱ������������ų�����CO2����һ�ִ�������Ч��ʽ��
��ͨ��O2�ɽ����Ժ�ˮ�е���(IV)�������÷�Ӧ�����ӷ���ʽ��_____________��
��������ʽʹ������ˮpH���ߵ�ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϩ����һ�������·���������Ӧ��̼̼˫�����ѣ��磺![]() ������Ϊ
������Ϊ![]() ��
��![]()
![]() ��
��![]() ��
��![]() ��
��![]() ��ʾ��������ԭ��
��ʾ��������ԭ��![]() ���ɴ��ƶϷ���ʽΪ
���ɴ��ƶϷ���ʽΪ![]() ��ϩ�����п��ܵ����������У� ��
��ϩ�����п��ܵ����������У� ��
A. 5��B. 6��C. 7��D. 8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���������ˮ�еμ�NaOH��Һ����Һ��ˮ�����![]() ��NaOH��Һ���֮��Ĺ�ϵ����ͼ��ʾ�������ƶ���ȷ���ǣ� ��
��NaOH��Һ���֮��Ĺ�ϵ����ͼ��ʾ�������ƶ���ȷ���ǣ� ��
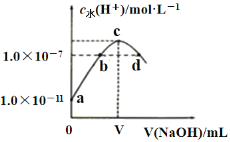
A. ��pH��ֽ�ⶨa���Ӧ��Һ����![]()
B. b��d���Ӧ����Һ�ж����ڣ�![]()
C. c���Ӧ����Һ�У�![]()
D. �����¼�ˮϡ��d���Ӧ����Һ����Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ��ǿ�ᣬŨ�ȳ���40��ʱ�ᷢ���ֽ⣬��Ӧ�ɱ�ʾΪ��a HClO3 = bO2��+ c Cl2��+ d HClO4 + e H2O�������й�˵����ȷ���� ( )
A. �ɷ�Ӧ��ȷ��������������HClO4
B. �ɷǽ�����Cl��S������֪����HClO3��H2SO4
C. ����ѧ������a=8��b=3����÷�Ӧת�Ƶ�����Ϊ8e��
D. ���÷�Ӧ����lmol�����������Ϊ45g����Ӧ�ɱ�ʾΪ��3HClO3 = 2O2��+ C12��+ HClO4 + H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��![]() ��Һ����
��Һ����![]() ��
��![]() ���ֽ�������
���ֽ�������![]() ������
������![]() ���Ũ�ȵĶ���ֵ
���Ũ�ȵĶ���ֵ![]() ��
��![]() �Ĺ�ϵ����ͼ������˵���д�����ǣ� ��
�Ĺ�ϵ����ͼ������˵���д�����ǣ� ��
A. ![]() ʱ��
ʱ��![]() ��
��![]() ��
��![]() С
С
B. ![]() ʱ��
ʱ��![]() ԼΪ
ԼΪ![]()
C. ![]() ��Һ�У�
��Һ�У�![]()
D. ��![]() Ũ��Ϊ
Ũ��Ϊ![]() �ķ�ˮ�м���
�ķ�ˮ�м���![]() ��ĩ������
��ĩ������![]() ��������
��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�������������ԭ��Ӧ���ǣ� ��
A.H2+Cl2=2HCl
B.2KMnO4![]() K2MnO4+MnO2+O2��
K2MnO4+MnO2+O2��
C.NH4HCO3![]() NH3��+CO2��+H2O
NH3��+CO2��+H2O
D.Zn+H2SO4=H2��+ZnSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
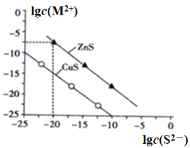
����Ŀ����ϸ��������һ����Ҫ�Ĺ����մ�ԭ�ϡ�
��1��ʵ���ҳ���NH4Al(SO4)2��NH4HCO3Ϊԭ�ϣ���һ���������ȷ�Ӧ���ɳ���NH4AlO(OH)HCO3���ó������·ֽ⼴�ó�ϸAl2O3��NH4AlO(OH)HCO3�ȷֽ�Ļ�ѧ��Ӧ����ʽΪ________________________________________________��
��2��NH4Al(SO4)2��12H2O����Է�������Ϊ453��������100 mL pHΪ2��Ũ��ԼΪ0.1 mol��L��1��NH4Al(SO4)2��Һ�����ƹ����������NH4Al(SO4)2��12H2O����_________g��
��3����0.1 mol��L��1 NH4Al(SO4)2��Һ�У�������̬��Ũ��(��Al3����)�Ķ���(lgc)����ҺpH�仯�Ĺ�ϵ����ͼ��
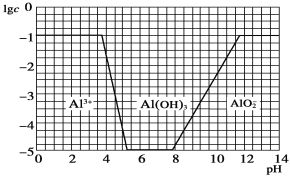
��NaOH��Һ���ڣ�2������ҺpH��7���ù����з�����Ӧ�����ӷ���ʽ��_______________________��_______________________��
��������(��Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO������)����ȡ�����������ֹ������̣�
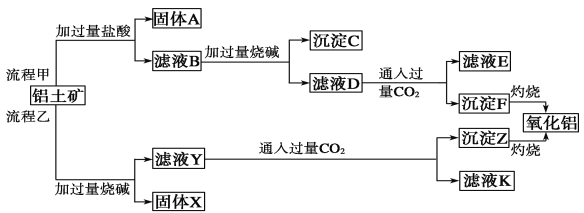
��ش��������⣺
��1�����̼������������Al3�������ӷ���ʽΪ_________________________��
��2������������ҺY��ͨ������CO2�����ӷ���ʽΪ_____________________��
��3����ҺE��K�����ʵ���Ҫ�ɷ���__________(�ѧʽ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com