
【题目】恒温、恒压下,1 mol A和1 mol B在一个容积可变的密闭容器中发生如下反应:A(g)+2B(g)![]() 2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
A. 物质A、B的转化率之比一定是1:2
B. 起始时刻和达到平衡后容器中的压强比为1:1
C. 若起始放入3 mol A和3 mol B,则达到平衡时生成3a mol C
D. 当v(正)(A)=v(逆)(B)时,可断定反应达到平衡
科目:高中化学 来源: 题型:
【题目】Mg、Al、Fe 三种金属的混合物与足量的稀硫酸反应,生成 2.8L H2(标准状况)则三种金属的物 质的量之和不可能是( )
A.0.12 molB.0.15 molC.0.09 molD.0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粮食仓储常用磷化铝(AlP)熏蒸杀虫,AlP遇水即产生强还原性的PH3气体。国家标准规定粮食中磷化物(以PH3计)的残留量不超过0.05mg·kg-1时为合格。某小组同学用图所示实验装置和原理测定某粮食样品中磷化物的残留量。C中加入100g原粮,E中加入20.00mL 2.50×10-4mol·L-1KMnO4溶液(H2SO4酸化),C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中的溶液。
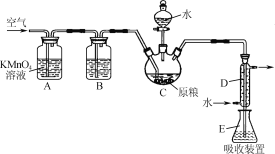
(1)装置A中的KMnO4溶液的作用是________。
(2)装置B中盛装焦性没食子酸的碱性溶液吸收空气中的O2。若去掉该装置,则测得的磷化物的残留量________(填“偏高”“偏低”或“不变”)。
(3)装置E中PH3被氧化成磷酸,MnO4-被还原为Mn2+,写出该反应的离子方程式:________。
(4)收集装置E中的吸收液,加水稀释至250mL,量取其中的25.00mL于锥形瓶中,用4.0×10-5 mol·L-1的Na2SO3标准溶液滴定,消耗Na2SO3标准溶液20.00 mL,反应原理是SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平)。通过计算判断该样品是否合格(写出计算过程)。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生可逆反应2NO(g)+O2(g)![]() 2NO2(g),不能说明该反应已经达到平衡状态的是
2NO2(g),不能说明该反应已经达到平衡状态的是
A. 正反应生成NO2的速率和逆反应生成NO的速率相等
B. 反应容器中压强不随时间的延长而变化
C. 混合气体颜色深浅保持不变
D. 混合气体的密度不随时间延长而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类化合物G是一种香料,以丙酮为初始原料合成该有机物的流程如下图所示(部分产物及反应条件已略去):
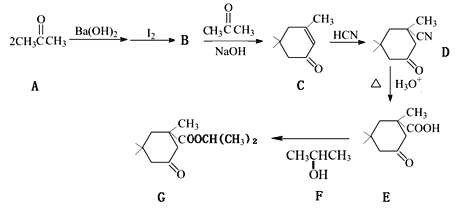
已知:![]()
(1)B的结构简式为______________,F的名称是__________。
(2)C中含氧官能团的名称是______________。
(3)C转化成D的反应类型_________________。
(4)D的分子式为_______________________。
(5)E转化成G的化学方程为________________。
(6)芳香化合物H比C少两个氢原子,能与氯化铁溶液反应显紫色且苯环上的一氯代物只有一种,写出满足上述条件的H的所有同分异构体的结构简式__________。H的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是____(填序号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(7)设计以CH3CH2CH2OH为起始原料制备2-甲基丙酸(![]() )的合成路线__(无机试剂任选)。
)的合成路线__(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验室用如图所示装置制取少量溴苯。请填写下列空白。

(1)在烧瓶a中装的试剂是苯、溴和铁屑。导管b的作用有两个:一是导气,二是兼起_______的作用。
(2)反应过程中在导管c的下口附近可以观察到白雾出现,这是由于反应生成的________遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有________生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色不溶于水的液体。这是溶解了溴的粗溴苯,可选用试剂 除去。
(5)写出烧瓶a中发生反应的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C三种无色溶液,它们分别是葡萄糖溶液、蔗糖溶液、淀粉溶液中的一种,某同学做实验得出:
①B能发生银镜反应;②A遇碘水变蓝色;③A、C均能发生水解反应,水解液均能发生银镜反应。
回答下列问题:
(1)写出各物质的名称:
A是________,B是________,C是________。
(2)写出有关化学反应方程式:
①蔗糖水解:__________________________________________。
②淀粉水解:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为了证明、比较SO2和氯水的漂白性,设计了如图所示的实验装置。

(1)实验室常选用KMnO4和浓盐酸制Cl2;选用Cu和浓硫酸反应制取SO2时,其中制SO2应选用如图A、E两发生装置中___装置(填装置序号),反应的化学方程式为___。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___,D:___。
(3)甲乙两名同学分别利用如图所示装置探究两种气体按不同比例混合后的漂白性。

试
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:___。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:___(结合反应方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富马酸二甲酯(DMF)俗称防霉保鲜剂霉克星1号,曾广泛应用于化妆品、蔬菜、水果等防霉、防腐、防虫、保鲜,它的一条合成路线如图所示。

回答下列问题:
(1)B的结构简式为______,D中官能团名称______。
(2)①的反应的类型是______,②的反应条件是______。
(3)④的反应方程式为______。
(4)写出C的一种同分异构体,满足可水解且生成两种产物可相互转化______。
(5)过程③由多个步骤组成,写出由C→D的合成路线_____。(其他试剂任选)(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com