
| A. | 1 mol NH4+ 所含质子数为10NA | |
| B. | 20 g氖气所含原子数约为6.02×1023 | |
| C. | 标准状况下,22.4 L SO2所含的分子数为NA | |
| D. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA |
分析 A.1个氨根离子含有10个电子;
B.氖气为单原子分子;
C.依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$=$\frac{V}{Vm}$计算解答;
D.氧气与臭氧都是由氧原子构成,依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$计算解答.
解答 解:A.1个氨根离子含有10个电子,1 mol NH4+ 所含质子数为10NA,故A正确;
B.20 g氖气所含原子数约为$\frac{20g}{40g/mol}$×6.02×1023=3.01×1023,故B错误;
C.标准状况下,22.4 L SO2所含的分子数为$\frac{22.4L}{22.4L/mol}$×NA=NA,故C正确;
D.常温常压下,32 g O2和O3的混合气体所含原子数为2$\frac{32g}{16g/mol}$×NA=2NA,故D正确;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意稀有气体为单原子分子.


科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl-、HS- | |
| B. | 酸性溶液中可能大量存在Na+、ClO-、SO42-、I- | |
| C. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×10-8 | 2×104 | 7×103 |
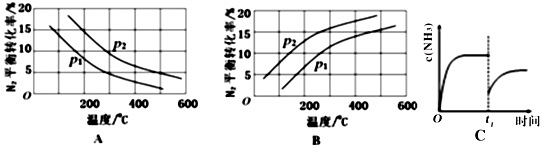
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ③ | C. | ②③ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:2:3 | C. | 3:2:1 | D. | 4:3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 标准状况下,22.4L的CCl4中含有CCl4分子数目为NA | |
| C. | 25℃时,1L 1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| D. | 6.4gCu与一定浓度的HNO3完全反应得到混合气体,转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强酸、强碱、大多数盐是强电解质,弱酸、弱碱和水是弱电解质 | |
| B. | 电解质溶液导电性的强弱跟单位体积溶液里自由移动的离子多少有关 | |
| C. | 具有强极性共价键的化合物一定是强电解质 | |
| D. | 硫酸钠是强电解质,碳酸氢钠也是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体就是直径为10-9m~10-7m的微粒 | |
| B. | 实验室制备Fe(OH)3胶体的方法是将饱和FeCl3溶液滴入NaOH溶液并加热 | |
| C. | 电解Fe(OH)3胶体,阴极附近红褐色加深,是因为胶体带正电,向阴极移动 | |
| D. | 可以用丁达尔效应来区别胶体和溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com