
【题目】研究电化学腐蚀及防护的装置如图所示.下列有关说法正确的是( ) 
A.锌片发生氧化反应作阴极
B.电子从铁片经过导线流向锌片
C.铁片上电极反应为:O2+2H2O+4e→4OH﹣
D.该装置可用于研究外加电流阴极保护法
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)下列各组物质: A.金刚石与石墨;B.淀粉与纤维素;C.氕与氘;D.甲烷与戊烷;E.葡萄糖与果糖
F. 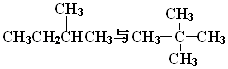 G.
G. 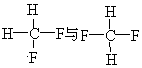
其中互为同位素的是(填编号,下同);互为同系物的是;互为同分异构体的是;是同一种物质的是 .
(2)化合物A的结构简式为: 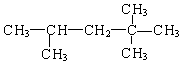 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含氢原子种类最少的一种结构简式为:;若A是由烯烃和H2通过加成反应得到,写出该烯烃的所有可能的结构简式 .
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含氢原子种类最少的一种结构简式为:;若A是由烯烃和H2通过加成反应得到,写出该烯烃的所有可能的结构简式 .
(3)篮烷分子的键线式如图所示,试回答: 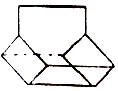
①写出篮烷分子的化学式;
②篮烷分子的一氯取代物的种数为种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,加入的先后顺序可以是( )
A.①②③④B.②③①④C.②①③④D.③②④①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1molCO2 的质量为44g/mol
B.物质的量就是物质的质量
C.气体摩尔体积约为22.4L/mol
D.NA个CO2的质量(以克为单位)与CO2的相对分子质量在数值上相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用.
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为、 . 某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图1: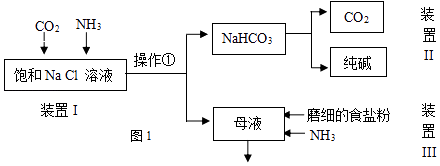
已知:几种盐的溶解度
NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
(2)①写出装置I中反应的化学方程式 . ②从平衡移动角度解释该反应发生的原因 .
③操作①的名称是 .
(3)写出装置II中发生反应的化学方程式 .
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用.
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是 . a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4 , 干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是向MgCl2、AlCl3混合溶液中,开始滴加7 mL试剂A,之后改滴加试剂B,所得沉淀物质的量y (mol) 与试剂体积V(mL)间的关系如图所示。(试剂A、B分别是NaOH 溶液盐酸中的一种)
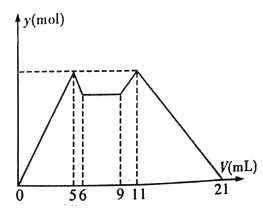
以下结论不正确的是
A. A是NaOH 溶液,B是盐酸
B. 原混合液中,c(Al3+) :c(Mg2+) :c(Cl-)=1:1:5
C. c(NaOH) :c(HCl)=1:2
D. 从6 到9 的过程中,发生的反应的离子反应方程式是H+ +OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
二 | C | N | ① | |||||
三 | ② | ③ | ④ | P | ⑤ | ⑥ |
请填写下列空白:
(1)表中元素,原子半径最大的是(填写元素符号);①的核外电子排布式;③和⑥两元素形成化合物的电子式为 .
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是(填化学式).
(3)比较④、⑤两种元素的简单离子半径:>(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为 .
(4)列举一个事实来证明元素①比元素⑤的非金属性强 .
(5)若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com