
【题目】据报道,我国科学家研制出以石墨烯为载体的催化剂,在 25℃下用 H2O2 直接将 CH4转化为含氧有机物,其主要原理如下图所示:
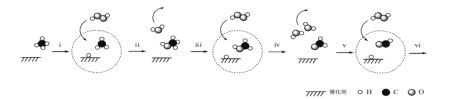
下列说法不正确的是
A.上图中 ![]() 代表 H2O2
代表 H2O2
B.由上图可知,步骤 iv 生成的 H2O,其中的 H 原子全部来自 H2O2
C.步骤 i、ii 的总反应方程式是CH4+H2O2![]() CH3OH+H2O
CH3OH+H2O
D.根据以上原理,推测步骤 vi 生成 HCOOH 和 H2O
科目:高中化学 来源: 题型:
【题目】利用如图完成一氧化氮与过氧化钠反应制备亚硝酸钠(2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3,NO能被酸性KMnO4溶液氧化为NO3-),下列说法错误的是

A.检查装置气密性后,应先打开止水夹,从导管中通入N2
B.装置C是用来吸收CO2的
C.D管中可能含有的杂质为NaNO3、NaOH
D.装置E用于处理尾气,反应中氧化剂与还原剂的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年10月1日是中华人民共和国成立70周年,国庆期间对大量盆栽鲜花施用了S-诱抗素制剂以保证鲜花盛开,S-诱抗素的分子结构简式如图。下列关于该物质的说法正确的是
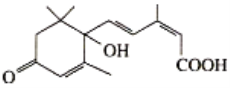
A.该有机物的分子式为C15H20O4
B.该有机物能发生取代、加成和水解反应
C.1mol的该有机物与足量的钠反应产生2molH2
D.1mol该有机物含有4mol双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据(已知![]() 为阿伏伽德罗常数的值):
为阿伏伽德罗常数的值):
试管中所加试剂及其用量/mL | 溶液退至无色所需时间/min | |||||
实验编号 | 实验温度/℃ | 0.6 mol/LH2C2O4溶液 | H2O | 3 mol/LH2SO4溶液 | 0.05 mol/LKMnO4溶液 | |
① | 25 | 3.0 | v1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | v2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式:___,当该反应以实验①中数据反应完全时转移电子数为_____![]() 。
。
(2)实验①②是探究浓度对反应速率的影响,实验②③时探究温度对反应速率的影响,则表中V1=_______,V2=__________。
(3)根据实验①、②的数据,可以得到的结论是____。
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。

该小组同学根据上述信息提出了新的假设,并设计一下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/ml | 再加入某种固体 | 溶液退至无色所需时间/min | |||
0.6 mol/LH2C2O4溶液 | H2O | 3 mol/LH2SO4溶液 | 0.05 mol/L KMnO4 溶液 | ||||
④ | 25 | 3.0 | 2.0 | 2.0 | 3.0 | MnSO4 | t |
①该小组同学提出的新假设是__________。
②若该小组同学提出的假设成立,应观察到__________(填实验现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a~n10中元素在周期表中的位置如图所示,请回答下列问题:
a | ||||||||
b | c | d | e | |||||
f | g | h | m | n | ||||
…… |
(1)m的阴离子的结构示意图为___。
(2)b的最高价氧化物的化学式为___;用化学方程式表示f、d的单质形成f2d2的过程___。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___(用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
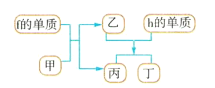
请写出h的单质与乙反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,利用 CO2 合成 CH3OH 的反应如下:CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g)△H1,研究发现,反应过程中会有副反应:CO2(g) + H2(g)
CH3OH(g) + H2O(g)△H1,研究发现,反应过程中会有副反应:CO2(g) + H2(g)![]() CO(g) + H2O(g) △H2。温度对 CH3OH、CO 的产率影响如图所示。下列说法中,不正确的是
CO(g) + H2O(g) △H2。温度对 CH3OH、CO 的产率影响如图所示。下列说法中,不正确的是
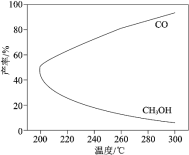
A.△H1 < 0,△H2 > 0
B.增大压强可以缩短合成反应达到平衡所需的时间
C.生产过程中,温度越高越有利于提高 CH3OH 的产率
D.合成 CH3OH 反应的平衡常数表达式是K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示内容的对应说明正确的是
编号 | A | B | C | D |
图示 |
食盐水 |
片刻后在Fe 电极附近滴入K3[Fe(CN)6]溶液 |
|
|
说明 | 验证铁钉发生 吸氧腐蚀 | 验证 Fe 电极被保护 | 该装置是牺牲阳极的阴极保护法 | 该化学反应为放热反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组利用文献资料设计方案对氯及其化合物进行探究。
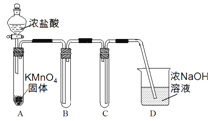
Ⅰ.用高锰酸钾和浓盐酸反应制取氯气
(1)该小组利用右图装置及试剂制备并收集适量Cl2,装置B、C的作用分别是___________、_______________。
(2)制得的氯气中加入适量水,得到饱和氯水,饱和氯水中含氯元素的微粒有____________(写出全部微粒)。
(3)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一。在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强。
①滤液漂白性增强的原因是________________(用化学平衡移动原理解释)。
②饱和氯水与石灰石反应生成HC1O的方程式是___________________。
Ⅱ. ClO3—、Cl—和H+反应的探究
(4)KClO3、KCl与硫酸可以反应。该小组设计了系列实验研究反应条件对反应的影响,实验记录如下(实验在室温下进行):
烧杯编号 | 1 | 2 | 3 | 4 |
氯酸钾饱和溶液 | 1mL | 1mL | 1mL | 1mL |
氯化钾固体 | 1g | 1g | 1g | 1g |
水 | 8mL | 6mL | 3mL | 0mL |
硫酸(6mol/L) | 0mL | 2mL | (____)mL | 8mL |
现象 | 无现象 | 溶液呈浅黄色 | 溶液呈黄绿色,生成浅黄绿色气体 | 溶液呈黄绿色, |
①该系列实验的目的_______________________。
②烧杯3取用硫酸的体积应为______________mL。
(5)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色。设计最简单的实验验证Cl2中含有ClO2______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的固定和氮的循环是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K 值。
反应 | 大气固氮N2(g)+O2(g) | 工业固氮N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:人类不适合大规模模拟大气固氮的原因____。
②从平衡视角考虑工业固氮应该选择常温条件,但实际工业生产却选择 500℃左右的高温, 解释其可能的原因_____。
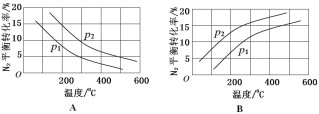
(2)工业固氮反应中,在其他条件相同时,分别测定 N2 的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,下图所示的图示中,正确的是_____(填“A”或“B”);比较р1、р2的大小关系_____。
(3)下图是某压强下,N2 与H2 按体积比1∶3投料时,反应混合物中氨的体积分数随温度的变化曲线。其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。
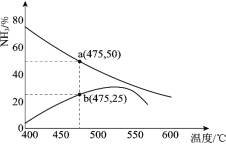
①图中b 点,v(正)_____v(逆)。(填“>”、“=”或“<”)
②图中a 点,容器内气体 n(N2):n(NH3)=_____。
(4)已知:N2(g)+3H2(g)![]() 2NH3(g)△H=-92.4kJ·mol-1;2H2(g) +O2(g)
2NH3(g)△H=-92.4kJ·mol-1;2H2(g) +O2(g)![]() 2H2O(l)△H=-575.6kJ·mol-1;近年,又有科学家提出在常温、常压、催化剂等条件下氮气与液态水合成氨气,同时产生氧气的新思路,则该反应的热化学反应方程式为:_____。
2H2O(l)△H=-575.6kJ·mol-1;近年,又有科学家提出在常温、常压、催化剂等条件下氮气与液态水合成氨气,同时产生氧气的新思路,则该反应的热化学反应方程式为:_____。
(5)NH3在一定条件下可被氧化。
已知:ⅰ.4NH3(g)+3O2(g)=2N2(g)+6H2O(g)ΔH=﹣1298kJ/mol
ⅱ.
① 断开 1 mol H-O 键与断开 1 mol H-N 键所需能量相差约_____kJ;
② H-O 键比 H-N 键(填“强”或“弱”)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com