

| A、图示中共有3种分子 |
| B、说明化学反应中原子不可分 |
| C、该图示不符合质量守恒定律 |
| D、该反应属于置换反应 |


科目:高中化学 来源: 题型:

| A、此图是1.0mol?L-1碳酸钠溶液滴定1.0 mol?L-1?HCl溶液的滴定曲线 |
| B、在pH分别为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-) |
| C、人体血液的pH约为7.4,则CO2在血液中多以HCO-3形式存在 |
| D、若用CO2和NaOH反应制取NaHCO3,应控制溶液的pH偏大或偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHSO3和NaHCO3的混合溶液中(S和C均用R表示):c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) |
| B、常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2,三种溶液中水的电离程度:③>①>② |
| C、39g Na2O2与足量水反应后转移的电子数为NA(NA表示阿伏加德罗常数的值) |
| D、当6.9g Fe3O4与足量稀HNO3反应(还原产物只有NO),则参加反应的HNO3为0.28mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对“地沟油”进行分馏可以获得汽油发动机的燃料 |
| B、乙烯和聚乙烯都可与溴水发生加成反应 |
| C、研究表明禽流感病毒H7N9在沸水中两分钟就能被杀死,是因为蛋白质受热易变性 |
| D、乙醇和乙酸的反应与苯和液溴的反应类型不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅和石墨都是重要的半导体材料 |
| B、SO2、NO2、CO2都会导致酸雨的形成 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理不同 |
| D、氢能是清洁能源,工业上用电解水法制大量氢气符合节能减排理念 |
查看答案和解析>>
科目:高中化学 来源: 题型:
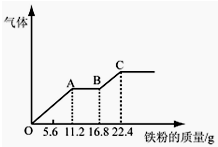 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A、原混合酸中NO3-物质的量浓度为2mol/L |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为2.5mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 对基苯甲醛,…俗称PHBA,是-种重要的有机化工原料.其结构如图所示
对基苯甲醛,…俗称PHBA,是-种重要的有机化工原料.其结构如图所示
查看答案和解析>>
科目:高中化学 来源: 题型:
 Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题:
Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com